-
Cuestión cinética química 0004
Explica de forma razonada por qué un aumento de la temperatura provoca un aumento mucho mayor de la velocidad de reacción.
-
Definición de conceptos de cinética química (570)
Explica brevemente el significado de los siguientes conceptos cinéticos:
a) Velocidad de reacción.
b) Ecuación de velocidad.
c) Energía de activación.
d) Orden de reacción.
-
Influencia de la temperatura en la velocidad de reacción (569)
En los envases de ciertos alimentos y medicamentos se puede leer la instrucción de conservar en lugar fresco o refrigerado. Razona el porqué de esta medida.
-
Velocidad de reacción, energía de activación y unidades de la constante de velocidad (568)
A 600 K, el valor de la constante de velocidad de la descomposición de una sustancia A es 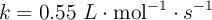 :
:
a) ¿Cuál es la velocidad de descomposición de la sustancia a esta temperatura si ![[A] = 3\cdot 10^{-3}\ \text{mol}\cdot L^{-1} [A] = 3\cdot 10^{-3}\ \text{mol}\cdot L^{-1}](local/cache-TeX/5b7c7f250126a5c4420a4ccc78983989.png) ?
?
b) Si a 625 K la constante de velocidad es 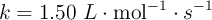 , ¿cuánto vale la energía de activación?
, ¿cuánto vale la energía de activación?
c) Fijándote en las unidades de la constante, ¿serías capaz de decir cuál es el orden de reacción de la descomposición de A?
-
Constante de velocidad y energía de activación (565)
La constante de velocidad de una reacción de primer orden es 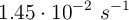 a
a 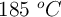 . ¿Cuál será su constante de velocidad a
. ¿Cuál será su constante de velocidad a 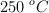 si la energía de activación del proceso es 12.35 kJ/mol?
si la energía de activación del proceso es 12.35 kJ/mol?
 RESUELTO
RESUELTO