-
Volumen final de un gas cuando se triplica su presión
Una cierta cantidad de gas, a 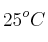 , ocupa un volumen de
, ocupa un volumen de 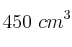 . ¿Cuál será su volumen final si la presión aumenta al triple del valor original, siendo constante la temperatura?
. ¿Cuál será su volumen final si la presión aumenta al triple del valor original, siendo constante la temperatura?
-
Volumen final de una masa de gas que se comprime a temperatura constante
Una cantidad de gas ocupa un volumen de 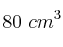 a una presión de 750 mm Hg. ¿Qué volumen ocupará a una presión de 1,2 atm si la temperatura no varía?
a una presión de 750 mm Hg. ¿Qué volumen ocupará a una presión de 1,2 atm si la temperatura no varía?
-
Volumen que ocupa un gas al ser calentado y aumentar su presión
En un recipiente de 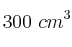 se introduce una cantidad de gas nitrógeno que ejerce una presión de 0,5 atm cuando se encuentra a
se introduce una cantidad de gas nitrógeno que ejerce una presión de 0,5 atm cuando se encuentra a 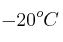 . ¿Qué volumen ocupará si, al calentarlo hasta
. ¿Qué volumen ocupará si, al calentarlo hasta 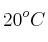 , llega a ejercer una presión de 900 mm Hg? Indica la ley de los gases que estás utilizando.
, llega a ejercer una presión de 900 mm Hg? Indica la ley de los gases que estás utilizando.
-
Determinación experimental de la constante de los gases ideales (5316)
En un intento por determinar un valor adecuado para la constante de los gases R, una estudiante calentó un recipiente de volumen 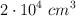 lleno con 0.25132 g de gas helio a
lleno con 0.25132 g de gas helio a 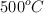 y midió la presión como 206.402 cm de agua en un manómetro a
y midió la presión como 206.402 cm de agua en un manómetro a 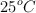 . Calcula el valor de R a partir de estos datos.
. Calcula el valor de R a partir de estos datos.
La densidad del agua a 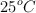 es
es 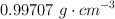 .
.
-
Trabajo de expansión isotérmica de un gas (5305)
Un recipiente contiene 525 libras de nitrógeno ocupando un volumen de 50 litros a una presión de 8 bar. Se expande isotérmicamente hasta que ocupe un volumen doble. Calcula:
a) La presión final.
b) La variación de la energía interna.
c) El trabajo realizado.
 Leyes de los gases
Leyes de los gases