-
Volumen que ocupan ciertos moles de un gas ideal
¿Cuál es el volumen, expresado en mL, que ocupa un gas ideal si 0.937 moles se encuentran a una temperatura de 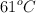 y a una presión de 3 709 mm Hg?
y a una presión de 3 709 mm Hg?
Dato: 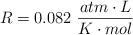
-
Número de globos que se pueden llenar con un tanque de helio (5235)
Un tanque de 10 L contiene He y se encuentra a una presión de 10 atm. Para inflar un globo de 1 L se requiere una presión un poco mayor que la atmosférica (1.0001 atm). ¿Cuántos globos se pueden inflar con el gas contenido en el tanque si la presión final dentro del tanque debe ser igual a la presión atmosférica? Considere la presión final del globo igual a 1.0001 atm.
-
Volumen final de un gas cuando varían la presión y la temperatura
La temperatura y presión iniciales de 2.1 mL de un gas son 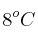 y 6.4 atm. Calcula el volumen final del gas cuando los valores de temperatura y presión son
y 6.4 atm. Calcula el volumen final del gas cuando los valores de temperatura y presión son 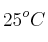 y 1 atm.
y 1 atm.
-
Masa de hidrógeno recogida a partir de datos de P, T y V
El hidrógeno gaseoso (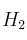 ), se forma por la reacción de calcio metálico (Ca) con agua, siendo recolectado en un dispositivo de recolección en agua. El volumen de gas recolectado a
), se forma por la reacción de calcio metálico (Ca) con agua, siendo recolectado en un dispositivo de recolección en agua. El volumen de gas recolectado a 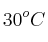 y una presión de 988 mm Hg es de 641 mL. ¿Cuál es la masa en gramos del
y una presión de 988 mm Hg es de 641 mL. ¿Cuál es la masa en gramos del 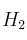 obtenido?
obtenido?
La presión de vapor del agua a 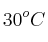 es de 31,82 mm Hg. (
es de 31,82 mm Hg. (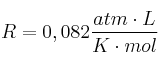 ; H = 1).
; H = 1).
-
Tiempo de difusión de 10 pies cúbicos de hidrógeno (5175)
¿Qué tiempo tarda en difundirse 10 pies cúbicos de hidrógeno, a través de una pared porosa, si el mismo volumen de oxígeno, en las mismas condiciones, tarda 10 minutos?
 Leyes de los gases
Leyes de los gases