-
Velocidad, orden de reacción y constante de velocidad 0001
En el estudio de la cinética de una reacción química se han realizado cuatro experimentos y se han obtenido los siguientes resultados, a 30 ºC:
![\begin{tabular}{| l | c | c | c | }
\hline &[A]o (M)&[B]o (M)&v (M/s)\\
\hline \hline Exp 1 &0,01&0,02&0,524\\
\hline Exp 2&0,01&0,06&4,716\\
\hline Exp 3&0,02&0,06&9,432\\
\hline Exp 4&0,04&0,02&2,096\\
\hline
\end{tabular} \begin{tabular}{| l | c | c | c | }
\hline &[A]o (M)&[B]o (M)&v (M/s)\\
\hline \hline Exp 1 &0,01&0,02&0,524\\
\hline Exp 2&0,01&0,06&4,716\\
\hline Exp 3&0,02&0,06&9,432\\
\hline Exp 4&0,04&0,02&2,096\\
\hline
\end{tabular}](local/cache-TeX/ceec65da86050c2d1183ff0da9c48e84.png)
Determina:
a) El orden total de reacción.
b) El valor de la constante de equilibrio a esa temperatura.
c) Si el proceso fuera elemental, ¿cuál sería su molecularidad?
-
Cuestión cinética química 0010
La reacción 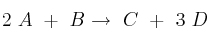 es un proceso elemental.
es un proceso elemental.
a) ¿Cuáles son los órdenes parciales y el orden total de reacción?
b) ¿Cuál es su ecuación cinética?
c) ¿Y su molecularidad?
d) Calcula la constante de velocidad si para concentraciones iniciales de A y B 0,1 M se ha obtenido un valor de la velocidad de 0,012 M/s.
-
Cuestión cinética química 0003
Define velocidad de reacción, orden de reacción y molecularidad. Explica sus posibles diferencias para el caso:
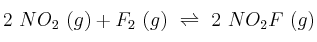
y justifica cómo se lograría aumentar más la rapidez de la reacción:
a) Duplicando la cantidad inicial de dióxido de nitrógeno.
b) Duplicando la cantidad inicial de flúor.
-
Ejercicio cinética química 0007
Para el siguiente equilibrio:
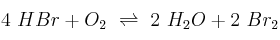
¿Crees que es posible que se trate de un proceso elemental en el coincidan, en la ecuación de velocidad, los órdenes parciales con los coeficientes estequiométricos? ¿Por qué?
-
Ejercicio cinética química 0004
Sabiendo que el proceso a A + b B → c C es elemental:
a) Escribe su ecuación de velocidad.
b) Indica sus órdenes parciales.
c) Escribe su orden total de reacción.
d) ¿Cuáles serán los valores más probables de los órdenes parciales? ¿Y la molecularidad del proceso?
 Molecularidad
Molecularidad