-
Ley de Hess: entalpía de formación del hexano (556)
Sabiendo que las entalpías estándar de combustión del hexano (l), del carbono (s) y del hidrógeno (g) son, respectivamente: -4 192 kJ/mol, -393.5 kJ/mol y -285.8 kJ/mol, calcula:
a) La entalpía de formación del hexano líquido en esas condiciones.
b) Los gramos de carbono consumidos en la formación del hexano cuando se han intercambiado 50 kJ.
-
PAU ley de Hess 0001
a) Escribe las ecuaciones de combustión del ácido butanoico, el hidrógeno y el carbón.
b) Indica cuáles de los reactivos o productos de esas reacciones tienen una entalpía de formación nula en condiciones estándar.
c) Aplicando la ley de Hess, explica cómo calcularías la entalpía de formación del ácido butanoico a partir de las entalpías de combustión de las reacciones del apartado a).
-
PAU entalpía 0005
La descomposición explosiva del trinitrotolueno 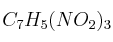 se puede expresar según:
se puede expresar según:
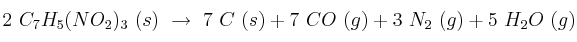
a) Halla la energía obtenida al descomponerse 1 kg de TNT.
b) Determina el volumen ocupado por los gases liberados en dicha descomposición, a presión atmosférica y a 500 ºC.
Datos: ![\Delta H^0_f[C_7H_5(NO_2)_3(s)] = -64,1\ kJ/mol \Delta H^0_f[C_7H_5(NO_2)_3(s)] = -64,1\ kJ/mol](local/cache-TeX/a98c721153dc3addc8105482e9a7138f.png) ;
; ![\Delta H^0_f[CO(g)] = -110,5\ kJ/mol \Delta H^0_f[CO(g)] = -110,5\ kJ/mol](local/cache-TeX/09ba8a60ad9cb82a43a37ba7bdeedb2a.png) ;
; ![\Delta H^0_f[H_2O(g)] = -241,8\ kJ/mol \Delta H^0_f[H_2O(g)] = -241,8\ kJ/mol](local/cache-TeX/121f649264d700ca0b3f070eca36e7dc.png) .
.
-
PAU entalpía 0004
El dióxido de manganeso se reduce a manganeso metal reaccionando con el aluminio según:
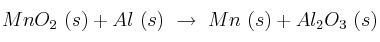
a) Halla la entalpía de esa reacción sabiendo que las entalpías de formación valen: 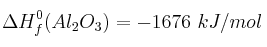 ;
; 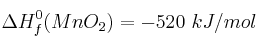
b) ¿Qué energía se transfiere cuando reaccionan 10 g de 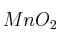 con 10 g de Al?
con 10 g de Al?
-
PAU entalpía 0003
A partir de la reacción de la fotosíntesis que realizan las plantas verdes:
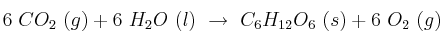
y sabiendo que 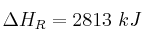 :
:
a) ¿Qué volumen de oxígeno, medido en condiciones estándar, se produce por cada gramo de glucosa formado?
b) Qué energía se requiere en ese proceso?
 Entalpía
Entalpía