-
Situación final de un vaso que contiene hielo y en el que se mete vapor de agua (6346)
En un vaso de cobre, cuya masa es de 1.5 kg, que contiene un bloque de hielo de 10 kg a la temperatura de 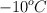 , se inyectan 5 kg de vapor de agua a
, se inyectan 5 kg de vapor de agua a 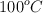 . Determina el estado de la mezcla.
. Determina el estado de la mezcla.
Datos: 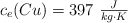 ;
; 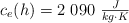 ;
; 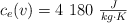 ;
; 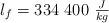
-
Calor de combustión de la xilosa a partir de la capacidad calorífica y la variación T (6262)
Teniendo en cuenta los siguientes datos, obtenidos en la combustión de una muestra de la xilosa ![[\ce{C5H10O5(s)}] [\ce{C5H10O5(s)}]](local/cache-TeX/4f6930c37d5be5f858a2e6b40b45c6d8.png) en un calorímetro de bomba, calcula el calor de combustión de la xilosa, expresado en kJ/mol:
en un calorímetro de bomba, calcula el calor de combustión de la xilosa, expresado en kJ/mol:
La masa de 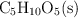 son 1.250 g, la capacidad calorífica del calorímetro es
son 1.250 g, la capacidad calorífica del calorímetro es 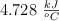 , la temperatura inicial del calorímetro es
, la temperatura inicial del calorímetro es 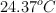 y la temperatura final del calorímetro es
y la temperatura final del calorímetro es 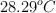 .
.
-
Capacidad calorífica de un calorímetro de bomba (6259)
Después de pasar por la combustión en un calorímetro de bomba, una muestra emite 5 435 cal. El calorímetro experimenta un aumento de 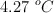 en su temperatura. Con esta información, determina la capacidad calorífica del calorímetro en
en su temperatura. Con esta información, determina la capacidad calorífica del calorímetro en 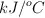 .
.
-
Capacidad calorífica de un calorímetro de bomba en el que se quema naftaleno (6258)
Determina la capacidad calorífica del calorímetro de bomba si la combustión de 1.714 g de naftaleno, 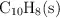 , provoca un aumento de la temperatura de
, provoca un aumento de la temperatura de 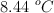 del sistema. El calor de combustión del naftaleno es
del sistema. El calor de combustión del naftaleno es 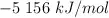 .
.
-
Calor necesario para calentar etanol hasta 150 grados centígrados (6211)
Calcula la cantidad de calor necesaria, expresada en kJ, para convertir 0.333 mol de etanol líquido a 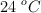 a etanol gaseoso a
a etanol gaseoso a 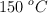 .
.
Datos: 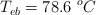 ;
; 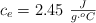 ;
; 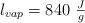 ;
; 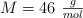
 Calor
Calor