-
Semirreacciones de oxidación y reducción en medios ácido y alcalino (6378)
Sin utilizar tablas de potenciales de reducción escribe las siguientes semirreacciones:
a) Reducción del manganeso en el 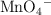 , a
, a 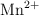 en medio ácido.
en medio ácido.
b) Oxidación del oxígeno del 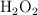 en medio ácido.
en medio ácido.
c) Reducción del azufre sólido en medio ácido.
d) Oxidación del azufre del 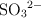 a
a 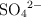 en medio alcalino.
en medio alcalino.
e) Reducción del 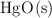 en medio alcalino.
en medio alcalino.
-
Reacción redox entre una aleación de cobre y ácido nítrico (6127)
Cuando se hacen reaccionar 200 g de una aleación, que contiene cobre en un 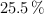 , con 180 mL de una disolución de ácido nítrico al
, con 180 mL de una disolución de ácido nítrico al 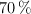 en masa y densidad 1.41 g/mL, se obtienen como productos de reacción óxido de nitrógeno(II), nitrato de cobre(II) y agua con un rendimiento del
en masa y densidad 1.41 g/mL, se obtienen como productos de reacción óxido de nitrógeno(II), nitrato de cobre(II) y agua con un rendimiento del 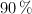 .
.
a) Ajusta la reacción que tiene lugar empleando el método del ion-electrón, indica cuál es el agente oxidante y el agente reductor, así como los estados de oxidación de las especies oxidadas y reducidas.
b) Calcula los gramos de nitrato de cobre(II) que se obtienen.
c) Si el óxido de nitrógeno(II) se recoge sobre agua a 293 K y 1 atm, calcula el volumen recogido.
Masas atómicas: Cu = 63.5 ; N = 14 ; O = 16 ; H = 1.
-
Balanceo de ecuaciones redox (6100)
Balancea las siguientes ecuaciones de oxidación-reducción:
a) 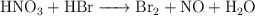
b) 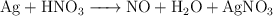
c) 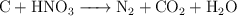
d) 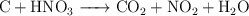
e) 
f) 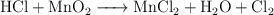
g) 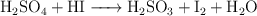
-
Volumen de disolución 0.1 normal de permanganato de sodio para valorar oxalato de sodio (6057)
¿Qué volumen de solución 0.1000 N de 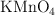 se necesitaría para valorar 0.1980 g de oxalato de sodio con una pureza del
se necesitaría para valorar 0.1980 g de oxalato de sodio con una pureza del 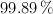 ?
?
-
Fórmula empírica a partir de la valoración redox de una muestra (5927)
Un compuesto contiene solamente Fe y O. Una muestra de 0.2729 g de este compuesto se disuelve en 50 mL de disolución ácida concentrada, reduciendo todo el hierro a iones 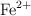 . La disolución resultante se diluye hasta 100 mL y se valora con una disolución 0.01621 M de
. La disolución resultante se diluye hasta 100 mL y se valora con una disolución 0.01621 M de 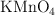 . La reacción química, sin ajustar, para la reacción es:
. La reacción química, sin ajustar, para la reacción es:

En la valoración se gastaron 42.17 mL de disolución de 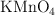 hasta alcanzar el punto final. ¿Cuál es la fórmula empírica del compuesto?
hasta alcanzar el punto final. ¿Cuál es la fórmula empírica del compuesto?
Masa atómica del Fe = 55.84.
 Ajuste redox
Ajuste redox