-
Equilibrio químico: Kp y presiones parciales 0001
Para la reacción: 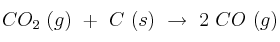 ,
, 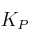 = 10 a la temperatura de 815 ºC. Calcule, en el equilibrio:
= 10 a la temperatura de 815 ºC. Calcule, en el equilibrio:
a) Las presiones parciales de 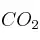 y CO a esa temperatura, cuando la presión total en el reactor es de 2 atm.
y CO a esa temperatura, cuando la presión total en el reactor es de 2 atm.
b) El número de moles de 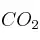 y de CO, si el volumen del reactor es de 3 litros.
y de CO, si el volumen del reactor es de 3 litros.
-
Equilibrio químico: Constantes de equilibrio Kc y Kp 0001
Una mezcla de 2,5 moles de nitrógeno y 2,5 moles de hidrógeno se coloca en un reactor de 25 L y se calienta a 400 ºC. En el equilibrio ha reaccionado el 5 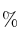 del nitrógeno. Calcula:
del nitrógeno. Calcula:
a) Los valores de las constantes de equilibrio  y
y 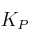 a 400 ºC, para la reacción
a 400 ºC, para la reacción 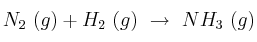
b) Las presiones parciales de los gases en el equilibrio.
-
PAU equilibrio químico 0012
A la temperatura de 400 ºC y 710 mm Hg de presión, el amoniaco se encuentra disociado en un 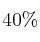 según la ecuación:
según la ecuación:
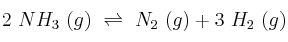
Calcula:
a) La presión parcial de cada uno de los gases que constituyen la mezcla en equilibrio.
b) El valor de las constantes 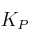 y
y  a esas temperaturas.
a esas temperaturas.
(Dato: 1 atm = 760 mm Hg)
-
PAU equilibrio químico 0006
A 350 ºC, el NOCl se descompone según la reacción:
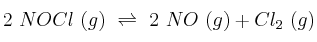
En el equilibrio, las presiones parciales de NOCl, NO y 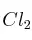 son, respectivamente, 307, 494 y 175 mm de Hg. Calcula la presión total en el equilibrio, el valor de
son, respectivamente, 307, 494 y 175 mm de Hg. Calcula la presión total en el equilibrio, el valor de 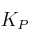 y el valor de
y el valor de  .
.
-
Problema equilibrio químico 0012
Para la reacción de descomposición del cloruro de amonio sólido:
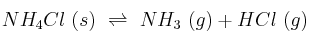
la constante de equilibrio, 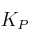 , es
, es 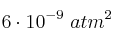 , a 400 K.
, a 400 K.
Calcula las presiones parciales de amoniaco y de cloruro de hidrógeno, producidos en la descomposición de una muestra de cloruro de amonio sólido, a 400 K, una vez alcanzado el equilibrio.
 Presión parcial
Presión parcial