-
EBAU Andalucía: química (junio 2022) - ejercicio B.3 (7923)
Dados los siguientes compuestos: 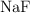 ,
, 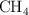 y
y 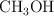 :
:
a) Justifica el tipo de enlace interatómico que presentan.
b) Ordénalos razonadamente de menor a mayor punto de ebullición.
c) Justifica la solubilidad de estos compuestos en agua.
-
Tipo de enlace, fórmula empírica y estructura de Lewis del compuesto entre Ga y C (7147)
En base al compuesto formado entre galio y carbono:
a) Indica qué tipo de unión se establece entre esos elementos, justificando tu conclusión.
b) ¿Cuál es el elemento que ganará electrones y cuántos serán? Justifica tu conclusión.
c) Halla la fórmula mínima y la estructura de Lewis del compuesto formado.
-
Afinidad electrónica del cloro con ciclo de Born-Haber (4776)
Mediante el ciclo de Born-Haber calcula la afinidad electrónica del cloro conociendo los siguientes valores energéticos:
Energía de sublimación del sodio = 78 kJ/mol.
Energía de ionización del sodio = 402 kJ/mol.
Energía de disociación del cloro = 160 kJ/mol.
Energía reticular del NaCl = - 760 kJ/mol.
Entalpía de formación del NaCl(s) = - 552 kJ/mol.
-
Carácter iónico de un enlace en función de la electronegatividad (4466)
A partir de los datos de la tabla, ¿cuál será el compuesto con mayor carácter iónico? ¿Por qué?
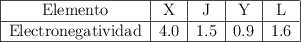
a) YJ.
b) YX.
c) LX.
d) JL.
-
Tipo de enlace en distintas sustancias (4323)
Relaciona cada uno de los grupos de términos según sea el tipo de enlace que se da en cada sustancia, puedes asignar más de un tipo a cada sustancia:
a) Covalente doble ; b) Covalente polar ; c) Covalente triple ; d) Iónico ; e) Covalente apolar ; f) Dativo ; g) Covalente simple.
1) oxígeno ; 2) bromuro de hidrógeno ; 3) sulfuro de magnesio ; 4) fluoruro de litio ; 5) nitrógeno ; 6) ácido carbónico.
 Iónico
Iónico