-
Moles de HCl para variar el pH de un búfer amonio/amoniaco (7475)
¿Cuántos moles de HCl se deben agregar a 1 L de una disolución amortiguadora, de concentraciones 0.84 M en amoniaco y 0.96 M en cloruro de amonio, para obtener una disolución de pH = 8.56? Supón que el volumen permanece constante.
Dato: 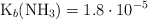
-
Fuerza iónica de un búfer de sales de fosfato (7242)
Calcula la fuerza iónica de una solución acuosa que contiene 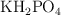 , con concentración
, con concentración 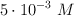 y
y 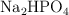 , con concentración
, con concentración 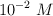 .
.
Datos: 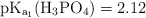 ;
; 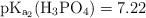 ;
; 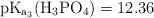
-
pH de un búfer de amoniaco y amonio (6608)
Se preparó una solución reguladora agregando a 1.0 L de solución de amoniaco, de concentración 3.4 g/L, cloruro de amonio en cantidad suficiente para que su concentración fuera 0.15 M. Calcula el pH de dicho amortiguador.
Dato: 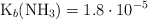 .
.
-
Volúmenes de ácido y sal del ácido para hacer una disolución reguladora de un pH dado
Se dispone de dos disoluciones: una 0.1 M de ácido acético y otra 0.1 M de acetato de sodio. ¿Qué volúmenes de cada una de ellas se deben mezclar para obtener 100 mL de una disolución reguladora de pH = 5.30?
Supón que los volúmenes son aditivos y toma como dato 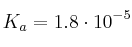 para el ácido acético.
para el ácido acético.
-
pH de una disolución de metilamina y pH del búfer formado al añadir cloruro de metilamonio (5518)
a) Se dispone de una disolución acuosa de metilamina 0.25 M. Sabiendo que su 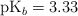 , ¿cuál es el pH de la disolución? Escribe la ecuación de disociación.
, ¿cuál es el pH de la disolución? Escribe la ecuación de disociación.
b) A 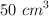 de la disolución anterior se le añaden
de la disolución anterior se le añaden 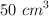 de una disolución 0.40 M de cloruro de metilamonio. Calcula el pH de la nueva disolución. Escribe el equilibrio que se establece y cómo actúa la mezcla búfer si se agrega NaOH.
de una disolución 0.40 M de cloruro de metilamonio. Calcula el pH de la nueva disolución. Escribe el equilibrio que se establece y cómo actúa la mezcla búfer si se agrega NaOH.
 Disolución tampón
Disolución tampón