-
KC y KP para una reacción sabiendo los moles iniciales y el grado de disociación (6727)
Se ha estudiado la reacción del equilibrio siguiente, a 735 K y en un volumen de un litro:
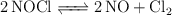
Inicialmente se introdujeron 2 moles de 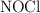 . Una vez alcanzado el equilibrio se comprobó que se había disociado en un
. Una vez alcanzado el equilibrio se comprobó que se había disociado en un 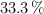 del compuesto. Calcula los valores de
del compuesto. Calcula los valores de 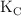 y
y 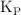 .
.
-
KP y KC de un equilibrio de disociación conocido el grado de disociación (6725)
A 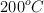 y presión de 1atm, el
y presión de 1atm, el 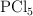 se disocia en
se disocia en 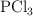 y
y 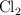 en un
en un 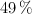 .Calcula:
.Calcula:
a) 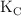 y
y 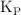 .
.
b) El grado de disociación a la misma temperatura pero a 10 atm de presión.
-
Presión parcial del CO a la que es letal
La hemoglobina (Hb) puede formar un complejo con 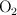 o con
o con 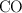 . Para la siguiente reacción, a temperatura corporal,
. Para la siguiente reacción, a temperatura corporal, 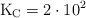 aproximadamente.
aproximadamente.

Cuando la relación ![\frac{[\ce{HbCO}]}{[\ce{HbO2}]} \frac{[\ce{HbCO}]}{[\ce{HbO2}]}](local/cache-TeX/3aab6fd7b82ea4d76fc01dd0b477bcb8.png) tiende a uno, la muerte es probable. ¿A qué presión parcial el
tiende a uno, la muerte es probable. ¿A qué presión parcial el 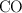 en el aire probablemente sea mortal? Asume que la presión parcial del
en el aire probablemente sea mortal? Asume que la presión parcial del 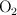 es 0.20 atm.
es 0.20 atm.
-
Presiones parciales y presión total en la descomposición del fosgeno
Para el equilibrio:
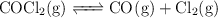
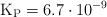 a determinada temperatura. Si al inicio la presión inicial del
a determinada temperatura. Si al inicio la presión inicial del 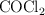 puro es 0.87 atm:
puro es 0.87 atm:
a) ¿Cuáles serán las presiones parciales en el equilibrio de 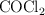 ,
, 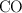 y
y 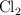 ?
?
b) ¿Cuál será la presión total en el equilibrio?
-
Concentración y masa inicial de un reactivo sabiendo la constante de equilbrio
En un recipiente de 5.00 L se introduce cloruro de amonio y se calientan a 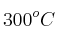 hasta que se alcanza el equilibrio, obteniendo como productos amoniaco y el ácido clorhídrico. Sabemos que en el equilibrio el amoniaco presenta una concentración de 0.92 mol/L y el ácido clorhídrico 1.40 mol/L. Si sabemos que
hasta que se alcanza el equilibrio, obteniendo como productos amoniaco y el ácido clorhídrico. Sabemos que en el equilibrio el amoniaco presenta una concentración de 0.92 mol/L y el ácido clorhídrico 1.40 mol/L. Si sabemos que 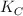 vale 0.0256:
vale 0.0256:
a) Plantea la ecuación química de la reacción en estudio.
b) Determina la concentración inicial y la cantidad química de cloruro de amonio de la cual se parte para que se dé la reacción.
 Constante equilibrio
Constante equilibrio