-
Cuestión equilibrio químico 0005
Las concentraciones en el equilibrio de las especies de la reacción 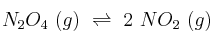 a 25 ºC, son 0,448 M para el reactivo y 0,0457 M para el producto. ¿Cuál es el rendimiento de la reacción?
a 25 ºC, son 0,448 M para el reactivo y 0,0457 M para el producto. ¿Cuál es el rendimiento de la reacción?
-
Problema equilibrio químico (392)
Cuando disolvemos zinc en ácido clorhídrico se obtiene un gas muy ligero como el hidrógeno. Si atacamos 3 g del metal con 85 mL del ácido (1.3 M) y la constante de equilibrio 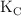 (a 298 K) es 0.831:
(a 298 K) es 0.831:
a) ¿Cuál es la concentración de cada especie en el equilibrio?
b) ¿Cómo reaccionaría el equilibrio si dejamos escapar parte del hidrógeno producido?
-
Concentración de producto conocida la constante de equilibrio (243)
En un recipiente de 2 L, a 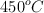 , se produce el equilibrio:
, se produce el equilibrio:
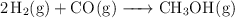
cuya 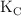 tiene un valor de 300. En el equilibrio hay 0.1 mol de
tiene un valor de 300. En el equilibrio hay 0.1 mol de 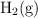 y 0.05 mol de
y 0.05 mol de 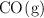 . Calcula la concentración de
. Calcula la concentración de 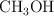 en el equilibrio, expresada en mol/L.
en el equilibrio, expresada en mol/L.
-
Constante de equilibrio para reacciones inversas (177)
La constante de equilibrio 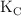 de la reacción:
de la reacción:

a 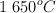 es 4.2. Determina la constante de equilibrio
es 4.2. Determina la constante de equilibrio 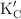 de la reacción:
de la reacción:

Razona tu respuesta, escribiendo la expresión de las constantes de equilibrio en cada caso.
-
Problema equilibrio químico: disociación del N2O4 (124)
A 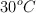 y 1 atm el
y 1 atm el 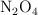 se encuentra disociado en un
se encuentra disociado en un 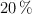 según el siguiente equilibrio:
según el siguiente equilibrio:

Calcula:
a) El valor de las constantes 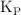 y
y 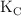 , a esa temperatura.
, a esa temperatura.
b) El porcentaje de disociación a 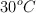 y 0.1 atm de presión total.
y 0.1 atm de presión total.
Dato: 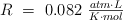 .
.
 Constante equilibrio
Constante equilibrio