-
Concentraciones en el equilibrio de la reacción entre nitrógeno y oxígeno
Para la ecuación química:
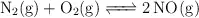
La constante de equilibrio 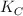 vale 0.00243 a 800 K. Si mezclamos 1.40 mol de
vale 0.00243 a 800 K. Si mezclamos 1.40 mol de 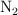 y 0.650 mol de
y 0.650 mol de 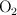 en un recipiente de 2.50 L a esa misma temperatura. Calcula la concentración para cada una de las especies en el equilibrio.
en un recipiente de 2.50 L a esa misma temperatura. Calcula la concentración para cada una de las especies en el equilibrio.
-
Concentraciones en equilibrio, Kc y Kp en la reacción de formación del amoniaco
En un recipiente de 10 L se introducen 1 mol de nitrógeno y 2 mol de hidrógeno, ambos en estado gaseoso, que se calientan hasta 618 K. Una vez que se alcanza el equilibrio, se obtiene una mezcla que ejerce una presión total de 9.48 atm según la reacción:
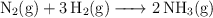
Calcula:
a) Las concentraciones de 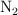 ,
, 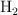 y
y 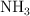 en el equilibrio.
en el equilibrio.
b) La  .
.
c) La 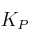 .
.
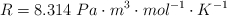
-
Valor de Kc y Kp la disociación del POCl3
En un recipiente de 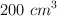 se colocan 0.4 g de
se colocan 0.4 g de 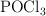 . Se calienta a
. Se calienta a 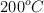 y el
y el 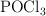 se vaporiza y se disocia en un
se vaporiza y se disocia en un 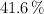 en
en 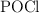 y
y 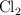 según el equilibrio:
según el equilibrio:
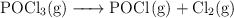
Calcula las constantes 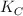 y
y 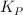 .
.
-
Constante de equilibrio a partir de los moles en el equilibrio
El hidrógeno gaseoso, el azufre en forma de vapor y el ácido sulfhídrico gaseoso se encuentran en equilibrio de acuerdo a la reacción:
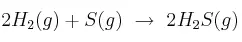
Si se tienen en el equilibrio 2 moles de 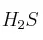 , 1,5 moles de
, 1,5 moles de 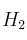 y
y 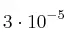 moles de S en un recipiente de 10 L a
moles de S en un recipiente de 10 L a  . ¿Cuál es el valor de
. ¿Cuál es el valor de  ?
?
-
Valor de KP para la disociación del SO3
El equilibrio entre 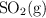 ,
, 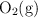 y
y 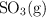 es importante en la producción de ácido sulfúrico. Se introducen 0.0200 mol de
es importante en la producción de ácido sulfúrico. Se introducen 0.0200 mol de 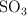 en un recipiente de 1.52 L a 900 K en el que se ha hecho vacío y, en el equilibrio, hay presencia de 0.0142 mol de
en un recipiente de 1.52 L a 900 K en el que se ha hecho vacío y, en el equilibrio, hay presencia de 0.0142 mol de 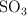 . Calcula el valor de
. Calcula el valor de 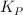 para la disociación del
para la disociación del 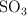 a 900 K.
a 900 K.
 Constante equilibrio
Constante equilibrio