-
Problema equilibrio químico 0005
En un recipiente de 10 L, a 800 K, se encierran un mol de CO (g) y un mol de vapor de agua. Cuando se alcanza el equilibrio:
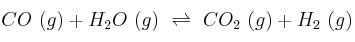
hay 0,665 moles de dióxido de carbono y 0,665 moles de hidrógeno gaseoso.
a) ¿Cuáles son las concentraciones de cada una de las especies en el equilibrio?
b) ¿Cuál es el valor de  para dicha reacción a 800 K?
para dicha reacción a 800 K?
-
Problema equilibrio químico 0004
En un matraz de 1 L hay 0,004 moles de 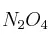 en equilibrio con 0,12 moles de
en equilibrio con 0,12 moles de 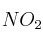 , a 373 K. Halla el valor de
, a 373 K. Halla el valor de  , a dicha temperatura, para el equilibrio:
, a dicha temperatura, para el equilibrio:
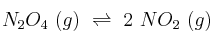
-
Problema equilibrio químico 0003
Se introducen, en un recipiente de 1,5 L, 0,300 moles de 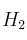 y 0,600 moles de
y 0,600 moles de 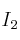 , a 350 ºC. Si la constante de equilibrio a esa temperatura es 38, ¿cuál es la concentración de cada especie en el equilibrio
, a 350 ºC. Si la constante de equilibrio a esa temperatura es 38, ¿cuál es la concentración de cada especie en el equilibrio 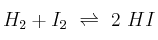 ?
?
-
Problema equilibrio químico (615)
Sabiendo que la 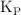 a
a 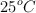 para la formación del amoniaco vale
para la formación del amoniaco vale 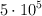 , calcula el valor de la nueva constante de equilibrio para una temperatura de
, calcula el valor de la nueva constante de equilibrio para una temperatura de 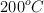 , sabiendo que la variación de entalpía del proceso es - 92 kJ.
, sabiendo que la variación de entalpía del proceso es - 92 kJ.
-
Cuestión equilibrio químico 0006
En un reactor de 3,5 L y a 200 ºC se hace reaccionar nitrógeno e hidrógeno para dar amoniaco. En un momento determinado la composición del sistema es 0,249 moles de 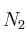 ,
, 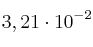 moles de
moles de 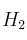 y
y 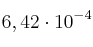 moles de
moles de 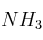 . Si la
. Si la  para la reacción a esa temperatura es 0,65, ¿habrá alcanzado el sistema el equilibrio? En caso de no estarlo, ¿hacia dónde evolucionará?
para la reacción a esa temperatura es 0,65, ¿habrá alcanzado el sistema el equilibrio? En caso de no estarlo, ¿hacia dónde evolucionará?
 Constante equilibrio
Constante equilibrio