El benceno y la piridina son líquidos a temperatura ambiente y se mezclan perfectamente entre sí, pero son inmiscibles con agua. Si mezclamos los tres líquidos, ¿cómo podríamos separarlos? Explica y describe cómo llevarías a cabo esa separación.
(Puntos de ebullición: benceno = ![]() ; piridina =
; piridina = ![]() ; agua =
; agua = ![]() ).
).
Imagina que haces una mezcla de azúcar y arena y luego la pones en un recipiente con agua y la agitas. ¿Qué componente se disolverá en el agua? ¿Cómo podrías volver a obtener los dos sólidos separados?
Explica cómo harías la separación de los componentes de una mezcla formada por limaduras de hierro, de aluminio, agua y etanol.
¿Qué método utilizarías para separar los indicado en las siguientes mezclas?
a) Las impurezas del agua.
b) La arena del ripio.
c) El agua de la sal.
d) El oro de la arena.
Indica el métodos de separación utilizado y la propiedad física en la que se basa la dicho método en cada una de las siguientes mezclas:
a) Hierro y azufre.
b) Agua y sal común.
c) Alcohol y vinagre.
d) Agua y aceite.
e) Mezcla de tintas.
Explica si las siguientes afirmaciones son verdaderas o falsas:
a) Generalmente las sustancias pueden distinguirse entre sí por sus propiedades intrínsecas.
b) Como la sal y el agua pueden separarse en sustancias más simples, la mezcla agua-sal es un compuesto.
c) Las disoluciones son mezclas heterogéneas.
A medio litro de agua se le añaden 35 g de ![]() a una temperatura de
a una temperatura de ![]() . Si la solubilidad de dicho compuesto a esa temperatura es 74.5 g de sal por cada 100 g de agua:
. Si la solubilidad de dicho compuesto a esa temperatura es 74.5 g de sal por cada 100 g de agua:
a) ¿Cómo es la disolución obtenida?
b) Para obtener una disolución saturada, ¿qué cantidad de soluto necesitaría?
c) ¿Qué cantidad de disolvente es necesaria para la disolución completa de los 35 g de soluto?
El agua tiene una temperatura de ![]() está en contacto con un gran volumen de aire a una presión total de 1 atmósfera:
está en contacto con un gran volumen de aire a una presión total de 1 atmósfera:
a) ¿Cuánto oxígeno está disuelto en el agua, expresado en ![]() ?
?
b) Supón que el agua incrementa su temperatura hasta los ![]() , ¿cuál es la nueva cantidad de oxígeno disuelto, en las mismas unidades?
, ¿cuál es la nueva cantidad de oxígeno disuelto, en las mismas unidades?
c) ¿Qué sucede si el agua a ![]() , teniendo una concentración inicial de oxígeno de
, teniendo una concentración inicial de oxígeno de ![]() , se expone al contacto con aire ordinario a la misma temperatura?
, se expone al contacto con aire ordinario a la misma temperatura?
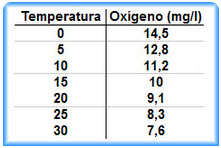
Utiliza la tabla de solubilidad adjunta:
Sobre una mesa de laboratorio hay tres frascos con la siguiente composición:
Frasco A. Contenido: ![]() de agua con 15 g de sulfato de sodio.
de agua con 15 g de sulfato de sodio.
Frasco B. Contenido: ![]() de agua con 14 g de sulfato de sodio.
de agua con 14 g de sulfato de sodio.
Frasco C. Contenido: ![]() de agua con 38 g de sulfato de sodio.
de agua con 38 g de sulfato de sodio.
Teniendo en cuenta que la solubilidad de la sal sulfato de sodio es ![]() , indica el tipo de disolución que contiene cada uno de los frascos:
, indica el tipo de disolución que contiene cada uno de los frascos:
a) El frasco A tiene en su interior una disolución: SATURADA - CONCENTRADA - DILUIDA
b) El frasco B tiene en su interior una disolución: SATURADA - CONCENTRADA - DILUIDA
c) El frasco C tiene en su interior una disolución: SATURADA - CONCENTRADA - DILUIDA
Se tiene el sistema formado por agua salada, mercurio y aceite. ¿Qué tipo de sistema es?
 Ejercicios FyQ
Ejercicios FyQ