Responde a las siguientes cuestiones justificando la respuesta:
a) ¿En qué grupo y en qué periodo se encuentra el elemento cuya configuración electrónica termina en ![]() ?
?
b) ¿Es posible el siguiente conjunto de números cuánticos (1, 1, 0, 1/2)?
c) ¿La configuración electrónica ![]() pertenece a un átomo en su estado fundamental?
pertenece a un átomo en su estado fundamental?
Escribe las configuraciones electrónicas de los siguientes elementos:
a) El elemento del grupo 14 de menor carácter metálico.
b) El elemento del tercer periodo de mayor radio atómico.
c) El elemento del cuarto periodo con solo un electrón en un orbital «d».
d) El elemento del segundo periodo que tiene más tendencia a formar un catión divalente.
Dadas las configuraciones electrónicas de tres elementos en estado fundamental $$$ X: [Ar]4s^2$$$, $$$ Y: [Ne]3s^23p^2$$$ y $$$ Z: [He]2s^22p^5$$$:
a) Determina su posición en la tabla periódica (periodo y grupo).
b) Indica nombre y símbolo de los elementos «Y» y «Z».
c) Justifica si es posible o no cada una de las siguientes combinaciones de números cuánticos. En los casos afirmativos, razona si puede corresponder al electrón más externo de alguno de los elementos del enunciado, indicando a cuál: (2, 1, 0, +½); (3, 0, 1, −½); (3, 2, 0, +½); (4, 4, 0, +½).
d) Define electronegatividad y justifica cuál de los elementos «X», «Y» o «Z» es el más electronegativo.
El ![]() del nitrógeno es
del nitrógeno es ![]() (masa isotópica 14.0031 u) y el resto es
(masa isotópica 14.0031 u) y el resto es ![]() (masa isotópica 15.0010 u). Determina el peso atómico del nitrógeno.
(masa isotópica 15.0010 u). Determina el peso atómico del nitrógeno.
Tres elementos tienen las siguientes configuraciones electrónicas:
![]() ;
; ![]() ;
; ![]()
La primera energía de ionización de estos elementos (no en ese orden) es ![]() ,
, ![]() y
y ![]() , y los radios atómicos son 97, 160 y 235 pm (
, y los radios atómicos son 97, 160 y 235 pm (![]() ):
):
a) Indica de qué elementos se tratan A y C.
b) Relaciona, de forma justificada, cada valor de energía con cada elemento.
c) Asigna, de forma justificada, a cada elemento el valor del radio correspondiente.
Dados los elementos Br, C, Cu y Li, ordénalos de forma creciente según: a) su radio atómico; b) su energía de ionización y c) su electronegatividad.
¿Cuál es la longitud de onda (en nanómetros) de la luz con una frecuencia de ![]() ?
?
¿Cuál es la frecuencia en (Hz) de la luz con una longitud de onda de 566 nm?
En la siguiente tabla se indican las energías de ionización (en eV) de tres elementos distintos:
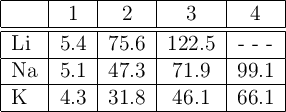
a) ¿Por qué la primera energía de ionización disminuye del litio al potasio?
b) ¿Por qué la segunda energía de ionización de cada elemento es mucho mayor que la primera?
c) ¿Por qué no se da el valor de la cuarta energía de ionización del litio?
Determina la frecuencia de la radiación emitida por un átomo de hidrógeno cuando un electrón transita desde la cuarta capa hasta la segunda.
Datos: ![]() ;
; ![]() .
.
 Ejercicios FyQ
Ejercicios FyQ