Una muestra gaseosa presenta un volumen de 5 litros partiendo de un volumen inicial de 0.65 litros. Si la variación de la temperatura ha oscilado desde a , ¿es posible esta variación del volumen para el gradiente de temperatura dado? Justifica tu respuesta mediante los cálculos correspondientes y enuncia la ley que usas para tu justificación.
Una carga ![]() ejerce una fuerza de 100 N sobre una carga de prueba
ejerce una fuerza de 100 N sobre una carga de prueba ![]() situada en un punto a 0,5 m de
situada en un punto a 0,5 m de ![]() :
:
a) ¿Cuál es el campo eléctrico que crea ![]() en dicho punto?
en dicho punto?
b) ¿Cuál es la magnitud de ![]() ?
?
Dato: 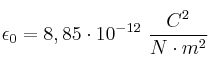
 EjerciciosFyQ
EjerciciosFyQ