-
PAU Andalucía: química (junio 2025) - pregunta 4 - ejercicio 4A (8488)
Nombra o formula los siguientes compuestos:
a) 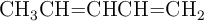 ; b)
; b) 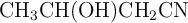 ; c) 3–metilpent-2-eno ; d) etanamida.
; c) 3–metilpent-2-eno ; d) etanamida.
-
PAU Andalucía: química (junio 2025) - pregunta 3 - cuestión 3B (8485)
Se preparan 250 mL de una disolución acuosa de 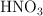 a partir de 2 mL de una disolución comercial de densidad
a partir de 2 mL de una disolución comercial de densidad 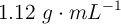 y
y 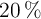 de riqueza en masa.
de riqueza en masa.
a) ¿Qué molaridad y pH tendrá la disolución preparada?
b) ¿Qué volumen de una disolución de NaOH 0.02 M será necesario añadir para neutralizar 100 mL de la disolución que se ha preparado?
Masas atómicas relativas: O= 16; N= 14; H= 1
-
PAU Andalucía: química (junio 2025) - pregunta 3 - ejercicio 3A (8479)
El equilibrio de descomposición del 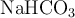 puede expresarse como:
puede expresarse como:
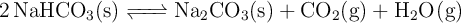
Para estudiar este equilibrio en el laboratorio, se depositaron 200 g de 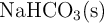 en un recipiente cerrado de 25 L, en el que previamente se hizo el vacío y se calentó a
en un recipiente cerrado de 25 L, en el que previamente se hizo el vacío y se calentó a 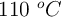 . La presión en el interior del recipiente, una vez alcanzado el equilibrio, fue de 1.65 atm. Calcula:
. La presión en el interior del recipiente, una vez alcanzado el equilibrio, fue de 1.65 atm. Calcula:
a) La masa de 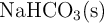 que queda en el recipiente tras alcanzarse el equilibrio a
que queda en el recipiente tras alcanzarse el equilibrio a 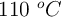 .
.
b) El valor de 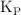 y
y 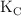 a esa temperatura.
a esa temperatura.
Dato: 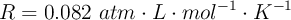 . Masas atómicas relativas: Na= 23; O= 16; C= 12; H= 1
. Masas atómicas relativas: Na= 23; O= 16; C= 12; H= 1
-
PAU Andalucía: química (junio 2025) - pregunta 2 - ejercicio 2B (8478)
La reacción química 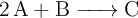 tiene como ecuación de velocidad
tiene como ecuación de velocidad ![v= k\cdot [A]^2\cdot [B] v= k\cdot [A]^2\cdot [B]](local/cache-TeX/054a83c6a1d414352e371e7095e78727.png) . Responde razonadamente:
. Responde razonadamente:
a) ¿Cuál es el orden total de la reacción?
b) Determina las unidades de la constante de velocidad.
c) ¿Se puede considerar que, durante el transcurso de la reacción química, la velocidad de la reacción permanece constante?
d) ¿La velocidad de desaparición de B es igual que la velocidad de aparición de C?
-
PAU Andalucía: química (junio 2025) - pregunta 2 - cuestión 2A (8477)
Justifica si son verdaderas o falsas las siguientes afirmaciones:
a) Un proceso exotérmico y espontáneo a cualquier temperatura tendrá 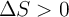 .
.
b) La sublimación del diyodo es un proceso que implica un aumento de entropía.
c) En todos los procesos espontáneos la entropía del sistema aumenta.
d) La reacción 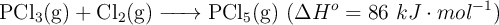 no es espontánea a ninguna temperatura.
no es espontánea a ninguna temperatura.
 RESUELTO
RESUELTO