-
PAU propiedad periódica 0004
Dados los elementos F, P, Cl y Na ordénalos de forma creciente según: a) sus radios atómicos; b) su energía de ionización; c) su electronegatividad.
-
PAU radiación electromagnética 0003
Si la energía de ionización del K gaseoso es de 418 kJ/mol:
a) Calcula la energía mínima que ha de tener un fotón para poder ionizar un átomo de K.
b) Calcula la frecuencia asociada a esta radiación e indica a qué región del espectro electromagnético pertenece.
c) ¿Podría ionizarse este átomo con luz de otra región espectral? Razona la respuesta. En caso afirmativo, indica qué zona del espectro sería.
-
Cuestión propiedad periódica (258)
La energía de ionización del catión 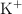 es mayor que la del átomo de argón,
es mayor que la del átomo de argón, 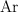 , a pesar de que ambas especies tienen 18 electrones. Explica el porqué de este hecho empírico.
, a pesar de que ambas especies tienen 18 electrones. Explica el porqué de este hecho empírico.
-
Selectividad Andalucía: química (junio 2009) - cuestión 2.A (112)
En la siguiente tabla se indican las energías de ionización (en eV) de tres elementos distintos:
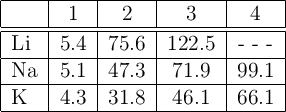
a) ¿Por qué la primera energía de ionización disminuye del litio al potasio?
b) ¿Por qué la segunda energía de ionización de cada elemento es mucho mayor que la primera?
c) ¿Por qué no se da el valor de la cuarta energía de ionización del litio?
 Energía ionización
Energía ionización