-
Selectividad junio 2013: propiedades periódicas
Para los siguientes elementos Na, P, S y Cl, diga razonadamente cuál es:
a) El de menor energía de ionización.
b) El de mayor afinidad electrónica.
c) El de mayor radio atómico.
-
Compuestos metálicos 0001
¿Cuál es el criterio, desde el punto de vista electrónico, que nos permite diferenciar un elemento metálico de otro que no lo es? ¿Cuál es su tendencia en el Sistema Periódico?
-
Propiedades periódicas: Radio atómico 0001
Las dos tablas siguientes corresponden a radios atómicos:
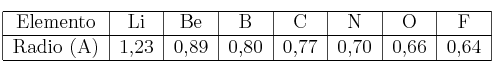
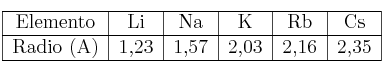
a) Justifica la variación del radio en el periodo.
b) Justifica la variación del radio en el grupo.
-
Configuración electrónica externa y propiedades periódicas 0001
Los elementos A y B tienen, en sus últimos niveles, las configuraciones:
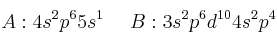
Justifica: a) si A es metal o no metal. b) Qué elemento tendrá mayor afinidad electrónica. c) Qué elemento tendrá mayor radio atómico.
-
Configuraciones electrónicas y tabla periódica 0001
Tres elementos tienen de número atómico 25, 35 y 38, respectivamente.
a) Escribe la configuración electrónica de los mismos.
b) Indica razonadamente el grupo y el periodo al que pertenece cada uno de los elementos anteriores.
c) Indica, razonando la respuesta, el carácter metálico o no metálico de cada uno de los elementos anteriores.
 Propiedades periódicas
Propiedades periódicas