-
Concentraciones en el equilibrio y constante de disociación 0001
Para el equilibrio 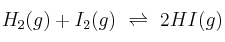 , la constante de equilibrio
, la constante de equilibrio  es 54,8 a la temperatura de 425 ºC. Calcula:
es 54,8 a la temperatura de 425 ºC. Calcula:
a) Las concentraciones de todas las especies en el equilibrio si se calientan, a la citada temperatura, 0,60 moles de HI y 0,10 moles de 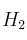 en un recipiente de un litro de capacidad.
en un recipiente de un litro de capacidad.
b) El porcentaje de disociación del HI.
-
Constantes de equilibrio: Dependencia de la temperatura 0001
A 613 K, el valor de  para la reacción:
para la reacción: 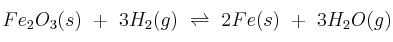 es 0,064. Si en el equilibrio anterior la presión parcial del hidrógeno es una atmósfera, calcula:
es 0,064. Si en el equilibrio anterior la presión parcial del hidrógeno es una atmósfera, calcula:
a) La concentración de hidrógeno.
b) La presión total.
-
Selectividad junio 2012: equilibrio químico, Kc y Kp
En una vasija de 10 L mantenida a 270 ºC y previamente evacuada se introducen 2,5 moles de pentacloruro de fósforo y se cierra herméticamente. La presión en el interior comienza entonces a elevarse debido a la disociación térmica del pentacloruro: 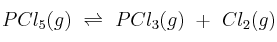 . Cuando se alcanza el equilibrio la presión es de 15,6 atm.
. Cuando se alcanza el equilibrio la presión es de 15,6 atm.
a) Calcula el número de moles de cada especie en el equilibrio.
b) Obtén los valores de 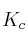 y
y 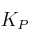 .
.
Dato: 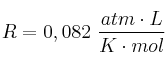
-
UNED: Equilibrio químico y cálculo de Kc
A una temperatura próxima a los 400 ºC se mezclan 0,062 mol de 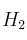 y 0,042 mol de
y 0,042 mol de 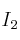 . Al establecerse el equilibrio se forman 0,076 mol de HI. Calcular:
. Al establecerse el equilibrio se forman 0,076 mol de HI. Calcular:
a) La constante de equilibrio  .
.
b) El número de mol de HI que se formará al mezclar, a la misma temperatura, 0,08 mol de 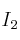 con 0,08 mol de
con 0,08 mol de 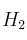 .
.
-
Equilibrio químico: Concentraciones en el equilibrio 0001
Si se introducen 0,100 moles de 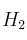 y 0,100 moles de
y 0,100 moles de 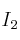 en un matraz de 10,0 L a 698 K. ¿Cuáles serán las concentraciones de equilibrio de
en un matraz de 10,0 L a 698 K. ¿Cuáles serán las concentraciones de equilibrio de 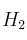 ,
, 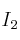 y HI?
y HI?  = 54,4 a 698 K.
= 54,4 a 698 K.
 Concentraciones
Concentraciones