-
PAU equilibrio químico 0013
Considera el siguiente sistema en equilibrio:
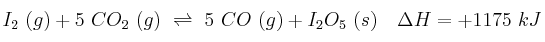
Justifica el efecto que tendrá, sobre el parámetro que se indica, el cambio que se propone:
a) Aumento de la temperatura (sobre el valor de  ).
).
b) Adición de 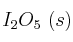 (sobre la cantidad de
(sobre la cantidad de 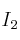 ).
).
c) Aumento de la presión (sobre la cantidad de CO).
-
PAU equilibrio químico 0008
El compuesto AB se disocia según la siguiente ecuación: 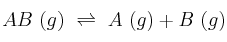 , con
, con 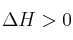 . Indica razonadamente qué le sucederá a una mezcla de los tres gases que experimenta las siguientes operaciones:
. Indica razonadamente qué le sucederá a una mezcla de los tres gases que experimenta las siguientes operaciones:
a) Aumentar la temperatura.
b) Disminuir el volumen.
c) Explica si alguno de los cambios anteriores hará aumentar o disminuir la constante de equilibrio.
-
PAU equilibrio químico 0007
Contesta brevemente a las siguientes cuestiones referidas a los equilibrios químicos:
a) ¿Para qué tipo de equilibrios se cumple que 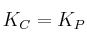
b) ¿Qué sucede en un equilibrio cuando se va extrayendo uno de los productos de la reacción según se va formando?
c) ¿En qué tipo de reacciones de equilibrio la constante aumenta al aumentar la temperatura?
-
PAU equilibrio químico 0003
En un recipiente de 0,5 L, y a cierta temperatura, se introducen 10 g de 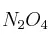 . Cuando se alcanza el equilibrio:
. Cuando se alcanza el equilibrio:
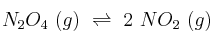
la constate  vale 0,182 M.
vale 0,182 M.
a) ¿Cuáles son las concentraciones en el equilbrio?
b) Suponiendo que la reacción es endotérmica, ¿será mayor  si aumentamos el valor de la temperatura del sistema? Razona tu respuesta.
si aumentamos el valor de la temperatura del sistema? Razona tu respuesta.
-
PAU equilibrio químico 0002
Una mezcla gaseosa constituida inicialmente por 3,5 moles de hidrógeno y 2,5 moles de yodo se calienta a 400 ºC, con lo que al alcanzar el equilibrio se obtienen 4,5 moles de HI, siendo el volumen del recipiente de 10 L. Calcula:
a) El valor de las constantes  y
y 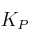 .
.
b) La concentración de los compuestos si el volumen se reduce a la mitad manteniendo constante la temperatura de 400 ºC.
 Le Chatelier
Le Chatelier