-
Masa de agua que se obtiene al mezclar masas distintas de hidrógeno y oxígeno (198)
Se hacen reaccionar 10 g de hidrógeno y 105 g de oxígeno para obtener agua. ¿Qué cantidad de agua será la que se obtenga?
Masas atómicas: H = 1 ; O = 16.
-
Ajuste de reacciones químicas sencillas (197)
Ajusta las siguientes reacciones:
a) 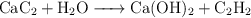
b) 
c) 
-
Estequiometría de las reacciones químicas, gases y disoluciones (106)
El cobre reacciona con ácido sulfúrico produciendo sulfato de cobre(II), dióxido de azufre y agua.
a) ¿Qué volumen de ácido sulfúrico al 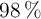 en peso y densidad 1.84 g/mL es necesario para obtener 100 L de dióxido de azufre, medidos en condiciones normales?
en peso y densidad 1.84 g/mL es necesario para obtener 100 L de dióxido de azufre, medidos en condiciones normales?
b) ¿Cuántos gramos de un mineral que contiene un 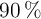 de pureza en cobre se necesitarán para obtener el volumen de dióxido de azufre anterior?
de pureza en cobre se necesitarán para obtener el volumen de dióxido de azufre anterior?
Datos: Cu = 63.5 ; S = 32 ; O = 16 ; H = 1.
-
Reacción entre el aluminio y el ácido clorhídrico (105)
El aluminio reacciona con el ácido clorhídrico dando cloruro de aluminio e hidrógeno. Se hacen reaccionar 100 g de una muestra de aluminio del 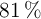 de pureza con ácido clorhídrico. Calcula:
de pureza con ácido clorhídrico. Calcula:
a) El volumen de disolución del ácido clorhídrico 5 M necesario para la reacción.
b) El volumen de hidrógeno gaseoso obtenido medido a 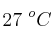 y 740 mm Hg.
y 740 mm Hg.
Datos: Al = 27 ; Cl = 35.45 ; H = 1.
-
Estequiometría: masa de hidruro de calcio para producir un volumen de hidrógeno (104)
El hidruro de calcio reacciona con el agua para formar hidróxido de calcio e hidrógeno:
a) Ajusta la reacción química.
b) ¿Cuántos gramos de hidruro de calcio harán falta para producir 5 L, en condiciones normales, de hidrógeno?
Datos: Ca = 40 ; H = 1.
 Reacciones químicas
Reacciones químicas