-
Ajuste redox en medio básico 0001
Ajusta la siguiente reacción redox por el método ion-electrón y calcula la masa de hidróxido de sodio que será necesaria para hacer reaccionar 35 g de la sal de cromo:
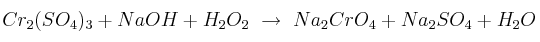
Datos: Cr = 52 ; S =32 ; O = 16 ; Na = 23 ; H = 1
-
Oxidación-reducción: Ajuste ion-electrón y estequiometría 0001
Una muestra de carbón de coque (C) de 10 g reacciona con ácido sulfúrico y se produce una mezcla de los siguientes gases: dióxido de azufre, dióxido de carbono y agua. Sabiendo que se han desprendido 35 L del óxido de azufre (1 atm y 25 ºC):
a) Indica quién es el agente reductor y quién el oxidante.
b) Ajusta la reacción por el método del ion-electrón.
c) ¿Cuál es la riqueza de la muestra de coque?
d) ¿Qué volumen de ácido sulfúrico 1,2 M será necesario para que reaccione la muestra?
-
Reacción redox: ajuste y estequiometría (1630)
El heptaoxidodicromato de dipotasio en presencia de ácido clorhídrico da la reacción:
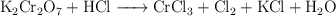
Calcula el volumen de dicloro que se obtendrá si se hacen reaccionar 15 g de 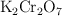 , con una riqueza del
, con una riqueza del 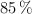 , con exceso de ácido, medidos a 1 atm y
, con exceso de ácido, medidos a 1 atm y 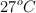 .
.
Datos: K =39 ; Cr = 52 ; O = 16.
-
Transferencia de electrones: ajuste y estequiometría 0001
El peróxido de hidrógeno es un oxidante fuerte que, en medio básico, es capaz de oxidar al cromo según la reacción:
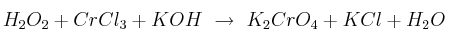
Calcula la cantidad de 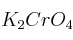 que se obtendrá a partir de 125 mL de disolución 0,2 M de la sal de cromo, si se hacen reaccionar con exceso del peróxido.
que se obtendrá a partir de 125 mL de disolución 0,2 M de la sal de cromo, si se hacen reaccionar con exceso del peróxido.
Datos: Cr = 52 ; K = 39 ; O = 16
-
Método ión-electrón 0001
Ajusta por el método ión-electrón la siguiente reacción en medio básico:
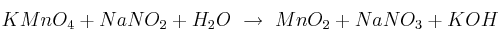
 Ajuste redox
Ajuste redox