-
Reacciones químicas: pureza de los reactivos 0002
Determina la pureza de una muestra de trioxidoclorato de potasio si 40 g de la misma, al descomponerse térmicamente en cloruro de potasio y dioxígeno, produjo 9,6 L de este último en c.n.
-
Reacciones químicas: estequiometría, disoluciones y gases 0001
El carbonato de magnesio reacciona con el trihidrógeno(tetraoxidofosfato) y da lugar al fosfato de magnesio, dióxido de carbono y agua.
a) Escribe la ecuación química.
b) Si se mezclan 22 g de carbonato de magnesio y 37 mL de ácido fosfórico (densidad = 1,34 g/mL y riqueza 50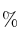 en peso), ¿qué volumen de dióxido de carbono se obtiene, medido a 23 ºC y una presión de 743 mm Hg.
en peso), ¿qué volumen de dióxido de carbono se obtiene, medido a 23 ºC y una presión de 743 mm Hg.
-
Problema de estequiometría 0009
El cinc es atacado por el ácido clorhídrico y su reacción desprende hidrógeno. Si una muestra de 15 g se hace reaccionar con ácido en exceso y libera 3,44 L de hidrógeno medidos a 27 ºC y 1 atm:
a) ¿Cuál es la riqueza de la muestra?
b) ¿Qué volumen de ácido 0,3 M haría falta para tratar 1,5 g de muestra?
Datos: Zn = 65,4 u ; Cl = 35,5 u ; H = 1 u ; R = 0,082 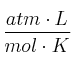
-
Problema reacciones 0012
Se hacen reaccionar 24 g de Fe y oxígeno en exceso para dar monóxido de hierro (FeO). ¿Qué cantidad del óxido obtendremos? ¿Qué volumen de 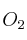 ha reaccionado, medido en condiciones normales?
ha reaccionado, medido en condiciones normales?
Datos: Fe = 56 ; O = 16
-
Problema reacciones 0011
Se hacen reaccionar 15,5 g de Cu con oxígeno en exceso para dar óxido cuproso (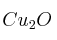 ). ¿Qué cantidad del óxido obtendremos? ¿Qué volumen de
). ¿Qué cantidad del óxido obtendremos? ¿Qué volumen de 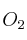 ha reaccionado, medido a 1,5 atm y 45 ºC? (Datos: Cu = 63,5 ; O =16)
ha reaccionado, medido a 1,5 atm y 45 ºC? (Datos: Cu = 63,5 ; O =16)
 Gases
Gases