-
Configuración electrónica y sistema periódico 0001
A partir de las siguientes configuraciones electrónicas, responde:
X: 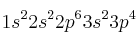 ; Y:
; Y: 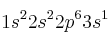 ; Z:
; Z: 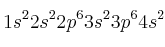
a) ¿A qué periodo y grupo pertenecen?
b) ¿Cuáles son sus números atómicos?
c) ¿Cuáles serán sus estados de oxidación más estables?
d) ¿Cuáles de esos iones serían isoelectrónicos?
-
Iones: Partículas atómicas y configuración electrónica 0001
Para los siguientes iones: 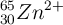 ;
; 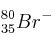 ;
; 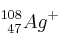 ;
; 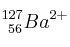 ;
; 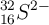
a) Indica el número de protones, neutrones y electrones.
b) Escribe sus configuraciones electrónicas.
-
Tabla periódica y configuración electrónica 0001
Indica razonadamente:
a) La posición en el sistema periódico y el estado de oxidación más probable de un elemento cuyos electrones de mayor energía poseen la configuración 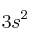 .
.
b) Si un elemento de configuración electrónica de su capa de valencia 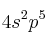 es un metal o no metal.
es un metal o no metal.
c) Por qué en los halógenos la energía de ionización disminuye a medida que aumenta el número atómico del elemento.
-
Configuración electrónica de iones estables 0001
Los números atómicos de los elemento Br y Rb son 35 y 37, respectivamente.
a) Escribe la configuración electrónica de ambos elementos.
b) Indica el ion más estable de cada elemento y su configuración electrónica.
c) Razona cuál de los dos iones tendrá mayor radio iónico.
-
Configuración electrónica y variación del radio iónico 0001
Los elementos Na, Al y Cl tienen números atómicos 11, 13 y 17, respectivamente:
a) Escribe la configuración electrónica de cada elemento.
b) Escribe la configuración electrónica de los iones 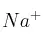 ,
, 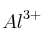 y
y 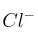 .
.
c) Ordene, de forma razonada, los radios de los iones anteriores.
 Número de oxidación
Número de oxidación