-
Calor de reacción en la formación de producto 0001
Dada la siguiente ecuación termoquímica:
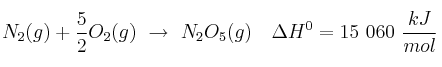
Calcula el calor (en kJ) que es absorbido durante la formación de 25,0 g de 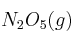 .
.
-
Selectividad junio 2013: entalpía de formación y entalpía de reacción
En la reacción del oxígeno molecular con cobre para formar óxido de cobre(II) se desprende 2,3 kJ por cada gramo de cobre que reacciona, a 298 K y 760 mm Hg. Calcula:
a) La entalpía de formación del óxido de cobre(II).
b) El calor desprendido a presión constante cuando reaccionan 100 L de oxígeno, medidos a 1,5 atm y 27 ºC.
Datos: R = 0,082 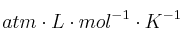 ; Masa atómica del Cu = 63,5.
; Masa atómica del Cu = 63,5.
-
Aplicación de la Ley de Hess 0001
Durante la combustión de 1 mol de átomos de azufre en condiciones estándar se desprenden 296,8 kJ y durante la combustión de 1 mol de sulfuro de hidrógeno, 560 kJ. Con estos datos, determina la variación de entalpía que se produce en el proceso.
-
Calor de combustión de un compuesto 0001
¿Cuál es la cantidad de energía que libera la combustión de 440 g de propano?
El calor de combustión del propano es -526 kJ/mol.
-
Entalpía estándar de formación y calor desprendido 0001
a) Calcula la variación de entalpía estándar de formación del acetileno (etino) a partir de las entalpías estándares de combustión (kJ/mol) de hidrógeno, C (grafito) y acetileno cuyos valores son, respectivamente: -285,3; -393,3 y -1298,3.
b) Calcula el calor desprendido, a presión constante, cuando se quema 1 kg de acetileno.
Masas atómicas: H = 1 ; C =12.
 Calor
Calor