-
Cuestión cinética química 0008
Las energías de activación para tres reacciones distintas son: 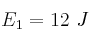 ;
; 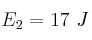 y
y 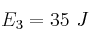 . Indica cuál de las tres reacciones es la más rápida y razona qué efecto tendrá en cada una de ellas un aumento de la temperatura.
. Indica cuál de las tres reacciones es la más rápida y razona qué efecto tendrá en cada una de ellas un aumento de la temperatura.
-
Cuestión cinética química 0007
La velocidad de reacción del proceso 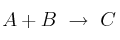 sigue la ecuación:
sigue la ecuación:
![v = k\ [A]^2[B] v = k\ [A]^2[B]](local/cache-TeX/13aec6ce51ed0e664884a61f239e742e.png)
A partir de estos datos responde a las siguientes cuestiones:
a) Indica el orden parcial de cada reactivo y el orden total de la reacción.
b) ¿Es un proceso bimolecular?
c) Si aumentamos la temperatura del sistema, ¿afectaría a esta reacción?
d) Si duplicamos la concentración inicial de A, ¿cómo variará la velocidad del proceso? ¿Y si triplicamos la concentración inicial de B?
-
PAU cinética química 0009
En la reacción 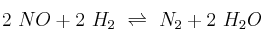 , a 1100 K, se obtuvieron los siguientes datos:
, a 1100 K, se obtuvieron los siguientes datos:
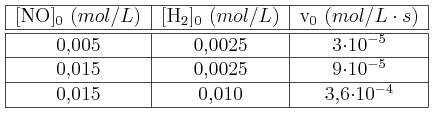
Velocidad reacción
Calcula el orden de reacción y el valor de la constante de velocidad.
-
PAU cinética química 0008
Mediante un diagrama de energía-coordenada de la reacción, justifica si la velocidad de reacción depende de la diferencia de energía entre:
a) Reactivos y productos, en cualquier estado de agregación.
b) Reactivos y productos, en su estado estándar.
c) Reactivos y estado de transición.
d) Productos y estado de transición.
-
PAU cinética química 0007
En la reacción 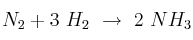 , el nitrógeno está reaccionando con una velocidad de 0,4 moles/minuto.
, el nitrógeno está reaccionando con una velocidad de 0,4 moles/minuto.
a) ¿A qué velocidad está reaccionando el hidrógeno? ¿Con qué velocidad se está formando el amoniaco?
b) ¿Con esos valores sería posible proponer valores adecuados para los exponentes 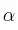 y
y 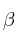 de la ecuación
de la ecuación ![v = k\ [N_2]^{\alpha}[H_2]^{\beta} v = k\ [N_2]^{\alpha}[H_2]^{\beta}](local/cache-TeX/fa2bc674a1ae8a9108ca814eb6f03ee5.png) o se necesitan más datos?
o se necesitan más datos?
 Velocidad reacción
Velocidad reacción