-
Ley de Boyle (1919)
Si introducimos cierta cantidad de gas en un recipiente de 2 L y lo cerramos herméticamente a una presión de 1 atm, ¿cuál será la presión final si reducimos el volumen a un tercio de litro? ¿Qué ley de los gases aplicas para resolver el problema? Considera que la temperatura es constante.
-
Leyes de los gases, moléculas y átomos 0001
Se dispone de tres recipientes que contienen en estado gaseoso 1 L de metano, 2 L de nitrógeno y 1,5 L de ozono (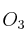 ) respectivamente, en las mismas condiciones de presión y temperatura. Justifica:
) respectivamente, en las mismas condiciones de presión y temperatura. Justifica:
a) ¿Cuál contiene mayor número de moléculas?
b) ¿Cuál contiene mayor número de átomos?
c) ¿Cuál tiene mayor densidad?
Masas atómicas: C = 12 ; N = 14 ; O = 16 ; H = 1
-
Mezcla de gases: mol, moléculas y átomos 0001
Se introducen 15 g de etano en una botella de 3 L de capacidad a 30 ºC:
a) ¿Cuál es la presión del gas en el recipiente?
b) ¿Cuántos átomos de hidrógeno hay?
c) Si los átomos presentes estuviesen todos libres, sin formar enlaces, y en estado gaseoso, ¿cuál sería la presión parcial del hidrógeno?
Datos: C = 12 ; H = 1 ; R = 0,082 atm·L/mol·K
-
Ley de Gay-Lussac: peligro de echar un bote de aerosol vacío al fuego
En el envase de cualquier aerosol podemos leer que no debemos arrojarlo al fuego ni aún vacío. ¿Por qué el fabricante está obligado a hacer esa advertencia? ¿En qué ley de los gases te basarías para explicar la advertencia?
-
Problema gases 0003
2,77 g de un gas ocupan 800 mL cuando están a 1,2 atm de presión y 27 ºC de temperatura. Determina la masa molecular del gas.
 Gases
Gases