-
Moles, átomos y moléculas 0001
Determina cuál de las muestras tiene mayor número de átomos: 0,75 g de dihidrógeno, 8,75 g de dinitrógeno o 17,4 L de helio, medidos a 25 ºC y 1 atm.
Datos: H = 1 ; N = 14 ; R = 0,082 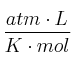
-
Mol, átomos, moléculas y número de Avogadro 0002
La estricnina 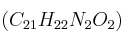 es un compuesto muy tóxico que se ha usado como raticida. Sin consideramos 15 g del compuesto:
es un compuesto muy tóxico que se ha usado como raticida. Sin consideramos 15 g del compuesto:
a) ¿Cuántos moles de carbono contiene? ¿Y de nitrógeno?
b) ¿Cuántas moléculas de estricnina?
c) ¿Cuántos átomos de hidrógeno?
-
Gases ideales (1560)
En un recipiente de 15 L se introducen 6 g de hidrógeno gaseoso y 55 g de diflúor. Si el sistema se calienta hasta los 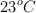 , ¿cuál será la presión? Si reducimos el volumen a la mitad, ¿cuál sería la nueva presión del sistema? (H = 1 ; F = 19).
, ¿cuál será la presión? Si reducimos el volumen a la mitad, ¿cuál sería la nueva presión del sistema? (H = 1 ; F = 19).
-
Gases ideales 0001
Se introducen 1,6 kg de dinitrógeno en un depósito de 750 L de volumen. Sabiendo que la presión máxima de seguridad es 3,5 atmósferas, ¿cuál será el valor máximo de temperatura que puede alcanzar el depósito, expresado en escala centígrada?
-
Mol y número de Avogadro 0001
Exprese en moles las siguientes cantidades de dióxido de carbono:
a) 11,2 L, medidos en condiciones normales.
b) 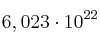 moléculas.
moléculas.
c) 25 L medidos a 27 ºC y 2 atmósferas.
Dato: R = 0,082 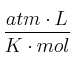
 Mol
Mol