-
Reacciones redox: Ajuste y estequiometría 0002
Dada la reacción redox en disolución acuosa:
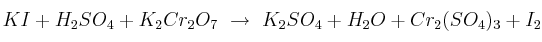
a) Ajuste por el método del ion-electrón la reacción.
b) Calcule la molaridad de la disolución de dicromato de potasio, si 30 mL de la misma reaccionan con 60 mL de una disolución que contiene 80 g/L de yoduro de potasio.
Masas atómicas: O = 16; K = 39; Cr = 52; I = 127
-
Redox: Método ion-electrón y estequiometría 0002
Dada la siguiente reacción redox en disolución acuosa:
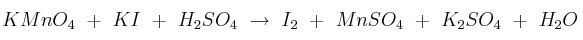
a) Ajustar la reacción por el método del ión-electrón.
b) Calcula los litros de disolución 2 M de permanganato de potasio necesarios para obtener 1 kg de yodo.
Masas atómicas: I = 127; K = 39; O = 16; Mn = 55
-
Reacción redox: ajuste y estequiometría 0003
En disolución acuosa y en medio ácido sulfúrico, el sulfato de hierro(II) reacciona con permanganato de potasio para dar sulfato de manganeso(II), sulfato de hierro(III) y sulfato de potasio.
a) Escribe y ajusta las correspondientes reacciones iónicas y la molecular del proceso por el método del ion-electrón.
b) Calcula la concentración molar de una disolución de sulfato de hierro(II) si 10 mL de esta disolución han consumido 22,3 mL de una disolución acuosa de permanganato de potasio 0,02 M.
-
Ajuste redox en medio básico 0001
Ajusta la siguiente reacción redox por el método ion-electrón y calcula la masa de hidróxido de sodio que será necesaria para hacer reaccionar 35 g de la sal de cromo:
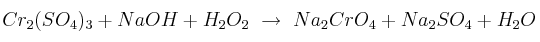
Datos: Cr = 52 ; S =32 ; O = 16 ; Na = 23 ; H = 1
-
Transferencia de electrones: ajuste y estequiometría 0001
El peróxido de hidrógeno es un oxidante fuerte que, en medio básico, es capaz de oxidar al cromo según la reacción:
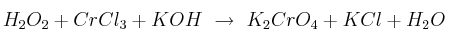
Calcula la cantidad de 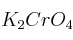 que se obtendrá a partir de 125 mL de disolución 0,2 M de la sal de cromo, si se hacen reaccionar con exceso del peróxido.
que se obtendrá a partir de 125 mL de disolución 0,2 M de la sal de cromo, si se hacen reaccionar con exceso del peróxido.
Datos: Cr = 52 ; K = 39 ; O = 16
 Ion-electrón
Ion-electrón