-
Selectividad junio 2013: propiedades periódicas
Para los siguientes elementos Na, P, S y Cl, diga razonadamente cuál es:
a) El de menor energía de ionización.
b) El de mayor afinidad electrónica.
c) El de mayor radio atómico.
-
Propiedades periódicas: Radio atómico 0001
Las dos tablas siguientes corresponden a radios atómicos:
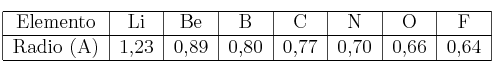
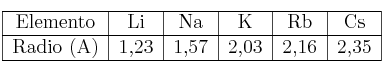
a) Justifica la variación del radio en el periodo.
b) Justifica la variación del radio en el grupo.
-
Configuración electrónica de iones estables 0001
Los números atómicos de los elemento Br y Rb son 35 y 37, respectivamente.
a) Escribe la configuración electrónica de ambos elementos.
b) Indica el ion más estable de cada elemento y su configuración electrónica.
c) Razona cuál de los dos iones tendrá mayor radio iónico.
-
Configuración electrónica externa y propiedades periódicas 0001
Los elementos A y B tienen, en sus últimos niveles, las configuraciones:
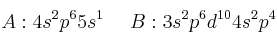
Justifica: a) si A es metal o no metal. b) Qué elemento tendrá mayor afinidad electrónica. c) Qué elemento tendrá mayor radio atómico.
-
Configuración electrónica y variación del radio iónico 0001
Los elementos Na, Al y Cl tienen números atómicos 11, 13 y 17, respectivamente:
a) Escribe la configuración electrónica de cada elemento.
b) Escribe la configuración electrónica de los iones 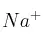 ,
, 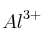 y
y 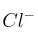 .
.
c) Ordene, de forma razonada, los radios de los iones anteriores.
 Radio atómico
Radio atómico