El dióxido de nitrógeno, a temperatura alta, se disocia en monóxido de nitrógeno y oxígeno:
![]()
Un recipiente metálico de 2,0 L de capacidad contiene solamente dióxido de nitrógeno a 25 ºC y 21,1 atm de presión. Se calienta el recipiente hasta 300 ºC, manteniéndose constante el volumen, y se observa que la presión de equilibrio en el recipiente es de 50 atm. Calcula, a 300 ºC:
a) El grado de disociación del ![]() .
.
b) El valor de ![]() para el equilibrio de disociación del
para el equilibrio de disociación del ![]() .
.
(Dato: 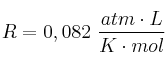 )
)
 EjerciciosFyQ
EjerciciosFyQ