-
Masa de agua que se obtiene al mezclar masas distintas de hidrógeno y oxígeno (198)
Se hacen reaccionar 10 g de hidrógeno y 105 g de oxígeno para obtener agua. ¿Qué cantidad de agua será la que se obtenga?
Masas atómicas: H = 1 ; O = 16.
-
Ajuste de reacciones químicas sencillas (197)
Ajusta las siguientes reacciones:
a) 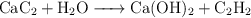
b) 
c) 
-
Problema sobre moles (196)
Determina las siguientes cantidades:
a) Átomos de sodio que hay en 10 g de sal común (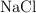 ).
).
b) Moles de potasio en 148 g de sulfuro de potasio (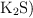 .
.
c) Átomos de hidrógeno en 5.2 g de metano (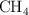 ).
).
-
Leyes de Proust y Lavoisier (195)
Hacemos reaccionar 38 g de cobre con oxígeno y se forman 47.57 g de óxido de cobre(II). Indica cuáles de estos procesos no son posibles y por qué:
a) 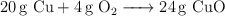
b) 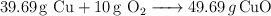
c) 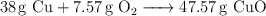
-
Leyes ponderales: leyes de conservación de la masa y de las proporciones definidas (193)
54 g de aluminio reaccionan con 96 g de 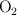 para formar el óxido de aluminio. ¿Qué cantidad de
para formar el óxido de aluminio. ¿Qué cantidad de 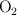 será necesaria para obtener 100 g de óxido? ¿Cuántos gramos de aluminio reaccionarán?
será necesaria para obtener 100 g de óxido? ¿Cuántos gramos de aluminio reaccionarán?
 RESUELTO
RESUELTO