-
Fórmula empírica de un hidrocarburo (4349)
Al quemar 5.20 mg de muestra de un hidrocarburo se obtuvieron 14.3 mg de 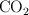 y 5.80 mg de
y 5.80 mg de 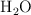 . Calcula la formula empírica del hidrocarburo.
. Calcula la formula empírica del hidrocarburo.
-
Fórmulas empírica y molecular a partir de composición centesimal (4286)
Una sustancia gaseosa contiene un 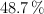 de carbono, un
de carbono, un 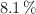 de hidrógeno y el resto de oxígeno. Si su masa molar es de 74 g/mol, determina cuáles son sus fórmulas empírica y molecular.
de hidrógeno y el resto de oxígeno. Si su masa molar es de 74 g/mol, determina cuáles son sus fórmulas empírica y molecular.
-
Fórmula empírica a partir de masas de elementos (3850)
En 3.63 g de un compuesto de oxígeno y calcio hay 2 g de calcio. Halla la formula empírica de este compuesto.
-
Fórmulas empírica y molecular de un compuesto (3617)
Una sustancia gaseosa contiene un 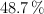 de carbono, un
de carbono, un 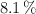 de hidrógeno y el resto de oxígeno. Si su masa molar es de 74 g/mol. Determina cuáles serán sus fórmulas empírica y molecular.
de hidrógeno y el resto de oxígeno. Si su masa molar es de 74 g/mol. Determina cuáles serán sus fórmulas empírica y molecular.
-
Moles de un elemento en fórmula empírica 0001
Si sabemos que hay 5 g de calcio en una muestra de cloruro de calcio, ¿cuántos moles de cloro habrá en la muestra?
 Fórmula empírica
Fórmula empírica