-
Reactivo limitante y masa de producto 0001
El nitrato de plata y el cloruro de calcio reaccionan en disolución. Todas las sustancias que intervienen en esta reacción son solubles en agua salvo el cloruro de plata, que forma un sólido (precipitado) que se sedimenta en el fondo del vaso de precipitado. Supón que mezclamos una disolución que contiene 9,54 g de nitrato de plata y otra que contiene 6,30 g de coluro de calcio. ¿Qué masa de cloruro de plata se formará?
-
Ajuste de reacción y concepto de mol 0001
¿Qué masa de pentano (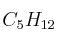 ) produce
) produce 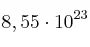 moléculas de
moléculas de 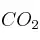 cuando se quema con oxígeno en exceso?
cuando se quema con oxígeno en exceso?
-
Relación estequiométrica en un reacción química 0001
Si 3 moles de 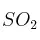 gaseoso reaccionan con oxígeno para producir trióxido de azufre, ¿cuántos moles de oxígeno se necesitan?
gaseoso reaccionan con oxígeno para producir trióxido de azufre, ¿cuántos moles de oxígeno se necesitan?
-
Reacción química: relación molar y másica entre sustancias 0001
En un alto horno, el trióxido de dihierro (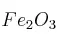 ) se hace reaccionar con carbón de coque (C) y se produce hierro fundido (Fe). Calcula el número de moles de hierro que se obtienen por cada kilogramo del óxido con que se alimente al horno. Escribe la ecuación química ajustada y obtén:
) se hace reaccionar con carbón de coque (C) y se produce hierro fundido (Fe). Calcula el número de moles de hierro que se obtienen por cada kilogramo del óxido con que se alimente al horno. Escribe la ecuación química ajustada y obtén:
a) La solución por el método de relación mol-mol.
b) La solución por el método de relación masa-masa.
-
Moles de producto y estequiometría en la combustión del amoniaco (2974)
De acuerdo con la reacción  , calcula cuántos moles de óxido de nitrógeno se obtienen a partir de 150 g de amoniaco.
, calcula cuántos moles de óxido de nitrógeno se obtienen a partir de 150 g de amoniaco.
Datos: N = 14 ; H = 1
 Ajuste
Ajuste