-
Refuerzo: masa de cobre al reaccionar hidrógeno y óxido de cobre(II) (6267)
Calcula la cantidad de cobre que se produce al reaccionar 400 mL de dihidrógeno, en condiciones normales, con un exceso de óxido de cobre(II). Los productos de la reacción son cobre y agua.
Considera la masa atómica del cobre como 63.5 g/mol.
-
Volumen de amoniaco al reaccionar 10 kg de nitrógeno (6149)
Una forma de sintetizar el gas amoniaco (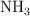 ) es combinando los gases nitrógeno y oxígeno a temperaturas y presiones extremadamente altas. Escribe la ecuación balanceada y calcula qué volumen de amoniaco se obtiene cuando 10 kg de nitrógeno se combinan con hidrógeno en exceso a
) es combinando los gases nitrógeno y oxígeno a temperaturas y presiones extremadamente altas. Escribe la ecuación balanceada y calcula qué volumen de amoniaco se obtiene cuando 10 kg de nitrógeno se combinan con hidrógeno en exceso a 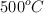 y 250 atm.
y 250 atm.
-
Estequiometría de reactivos y productos en la combustión de benceno
La combustión del benceno (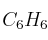 ) da como resultado la formación de dióxido de carbono y agua. Si se obtuvieron 25.8 L de dióxido de carbono, medidos en condiciones normales, calcula:
) da como resultado la formación de dióxido de carbono y agua. Si se obtuvieron 25.8 L de dióxido de carbono, medidos en condiciones normales, calcula:
a) Los gramos de agua que se formaron.
b) El volumen de benceno que reaccionó.
c) El volumen del aire, medido a 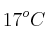 y 0.86 atm, que se necesitó.
y 0.86 atm, que se necesitó.
Considera que la densidad del benceno es igual a 0.88 g/mL y que el contenido de oxígeno en el aire es del  en volumen.
en volumen.
-
Volumen de hidrógeno que se obtiene al reaccionar níquel con ácido nítrico (5810)
Se hace reaccionar en un recipiente 23.5 g de una lámina de níquel metálico con acido nítrico al 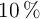 (m/V) según la reacción:
(m/V) según la reacción:
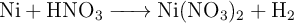
a) ¿Qué volumen de 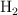 , a una presión de 912 mm Hg y a
, a una presión de 912 mm Hg y a 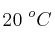 , se obtiene si la reacción se produce con un rendimiento del
, se obtiene si la reacción se produce con un rendimiento del 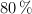 ?
?
b) ¿Qué volumen mínimo necesito agregar al recipiente para que se produzca la reacción?
-
Volumen de dióxido de carbono que se obtiene al quemar carbono (5763)
¿Qué volumen de 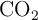 , medido a
, medido a 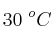 y 1.25 atm, se producirá al quemar 12 g de carbono en un ambiente saturado de
y 1.25 atm, se producirá al quemar 12 g de carbono en un ambiente saturado de 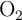 ?
?
 Gases
Gases