-
Masa de agua e hidróxido de calcio en la reacción del CaO con agua (7010)
Cuando el óxido de calcio reacciona con agua se forma hidróxido de calcio y se desprende energía.
a) ¿Qué masa de agua se necesita para que reaccionen 120 g de óxido de calcio?
b) ¿Cuántos moles de hidróxido de calcio se obtendrán?
Masas atómicas: Ca = 40 ; H = 1 ; O = 16.
-
Masa de hidrógeno y moléculas de nitrógeno al descomponer amoniaco (7009)
El amoniaco se descompone dando lugar a hidrógeno y nitrógeno, siendo todas las sustancias gaseosas. Si se introducen en un recipiente 32 L de amoniaco, medidos en condiciones normales:
a) ¿Qué masa de hidrógeno se obtendrá en las mismas condiciones?
b) ¿Cuántas moléculas de nitrógeno se forman?
Datos: N = 14 ; H = 1 ; 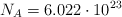
-
Volumen de CO2 y masa de H2O en la combustión del etano (7005)
Cuando el etano (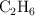 ) se quema con oxígeno se producen dióxido de carbono y agua. Si el proceso se da en condiciones normales, calcula:
) se quema con oxígeno se producen dióxido de carbono y agua. Si el proceso se da en condiciones normales, calcula:
a) El volumen de dióxido de carbono que se obtiene al quemar 80 g de etano.
b) La masa de agua que se produce.
Masas atómicas: C = 12 ; H = 1 ; O = 16.
-
Relación másica y moles de producto en la reacción de un ácido con un metal (7004)
La reacción entre el ácido clorhídrico y el cinc, en medio acuoso, produce cloruro de cinc e hidrógeno gaseoso. Si tras la reacción se recogen 12.5 L de hidrógeno, medidos en condiciones normales, calcula:
a) La masa de cada reactivo que ha reaccionado.
b) Los moles de cloruro de cinc producidos.
Masas atómicas: Zn = 65.4 ; H = 1 ; Cl = 35.5
-
Masa de cromo y moléculas de óxido de aluminio que se obtienen tras reacción (6997)
Cuando el óxido de cromo(III) reacciona con aluminio se forman el óxido de aluminio y cromo metálico. Si se hacen reaccionar 125 g de óxido de cromo(III) con exceso de aluminio:
a) ¿Qué masa de cromo se obtiene?
b) ¿Cuántas moléculas de óxido de aluminio se formarán al final de la reacción?
Datos: Al = 27 ; O = 16 ; Cr = 52 ; 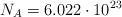 .
.
 EDICO
EDICO