-
Normalidad y molaridad de una disolución de HCl sabiendo su densidad y porcentaje en masa
Se dispone de ácido clorhídrico de densidad 1,2 g/mL y 39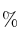 (m/m) de concentración. Calcula la normalidad y la molaridad de la disolución.
(m/m) de concentración. Calcula la normalidad y la molaridad de la disolución.
-
Neutralización: reactivos con formas distintas de concentración (2838)
Se hacen reaccionar 100 mL de ácido fosfórico 3 N con un volumen determinado de hidróxido de sodio 2.5 M para producir fosfato de sodio. Si las proporciones son estequiométricas:
a) ¿Cuál debe ser el volumen de hidróxido de sodio a agregar?
b) Suponiendo que los volúmenes de las soluciones son aditivos, ¿cuál es el porcentaje (m/V) de la sal formada en la solución al final de la reacción?
-
Molaridad de una disolución de sacarosa 0002
Calcular la molaridad de una solución que contiene 3,42 g de sacarosa (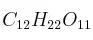 ) en un volumen de 200 mL.
) en un volumen de 200 mL.
-
Estequiometría en reacción de neutralización (2689)
En un recipiente se mezclaron 300 mL de disolución de ácido bromhídrico (HBr) 0.25 M con 750 mL de disolución 0.1 M de hidróxido de potasio (KOH). Los gramos de bromuro de potasio (KBr) (M=119 u) obtenidos en la mezcla fueron:
a) 0.46 g
b) 4.6 g
c) 8.9 g
d) 0.89 g
-
Concentración g/L y molaridad 0001
Se disuelven 10 mol de azúcar (sacarosa), cuya masa molar es 342 g/mol, en suficiente agua para formar 5,0 L de disolución:
a) ¿Cuál es la molaridad de la disolución?
b) Expresa la concentración en g/L.
 Molaridad
Molaridad