-
Entalpía de reacción a partir de entalpías de formación 0002
Determina el valor de las entalpías de las siguientes reacciones:
a) 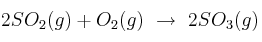
b) 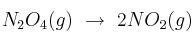
Datos: Entalpías de formación en kJ/mol: 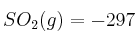 ;
; 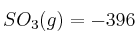 ;
; 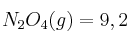 ;
; 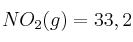
-
PAU Andalucía junio 2014: energía de reacción y calor intercambiado
Para la obtención del tetracloruro de carbono según: 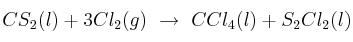 :
:
a) Calcula el calor de reacción, a presión constante, a 25 ºC y en condiciones estándar.
b) ¿Cuál es la energía intercambiada en la reacción anterior, en las mismas condiciones, cuando se forma un litro de tetracloruro de carbono cuya densidad es 1,4 g/mL?
Datos: ![\Delta H_f^0[CS_2(l)] = 89,70\ kJ/mol \Delta H_f^0[CS_2(l)] = 89,70\ kJ/mol](local/cache-TeX/8b2f589700663f467dafdacb3359026e.png) ;
; ![\Delta H_f^0[CCl_4(l)] = -135,40\ kJ/mol \Delta H_f^0[CCl_4(l)] = -135,40\ kJ/mol](local/cache-TeX/9bea697cf75cffedef11777a6f9d718e.png) ;
; ![\Delta H_f^0[S_2Cl_2(l)] = -59,80\ kJ/mol \Delta H_f^0[S_2Cl_2(l)] = -59,80\ kJ/mol](local/cache-TeX/cc5fa7d0201585381e2b07f14bb8f47b.png) ; Masas atómicas: C = 12 ; Cl = 35,5
; Masas atómicas: C = 12 ; Cl = 35,5
-
Calor de combustión por gramo 0001
La concentración de 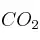 en la atmósfera está aumentando de forma constante debido al uso de combustibles fósiles cómo fuente de energía y es teóricamente posible demostrar que este hecho es el causante de producir un incremento de la temperatura de la Tierra (efecto invernadero).
en la atmósfera está aumentando de forma constante debido al uso de combustibles fósiles cómo fuente de energía y es teóricamente posible demostrar que este hecho es el causante de producir un incremento de la temperatura de la Tierra (efecto invernadero).
Escribe las reacciones balanceadas de combustión de los siguientes combustibles:
a) Hidrógeno (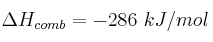 )
)
b) Propano (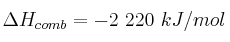 )
)
c) Metano (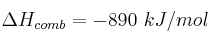 )
)
Indica razonadamente cuál de ellos desprende mayor cantidad de calor por gramo quemado y cuál es el que menos contamina.
-
Calor de reacción en la formación de producto 0001
Dada la siguiente ecuación termoquímica:
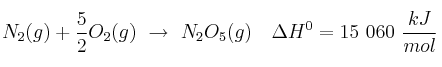
Calcula el calor (en kJ) que es absorbido durante la formación de 25,0 g de 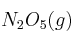 .
.
-
Selectividad junio 2013: entalpía de formación y entalpía de reacción
En la reacción del oxígeno molecular con cobre para formar óxido de cobre(II) se desprende 2,3 kJ por cada gramo de cobre que reacciona, a 298 K y 760 mm Hg. Calcula:
a) La entalpía de formación del óxido de cobre(II).
b) El calor desprendido a presión constante cuando reaccionan 100 L de oxígeno, medidos a 1,5 atm y 27 ºC.
Datos: R = 0,082 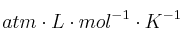 ; Masa atómica del Cu = 63,5.
; Masa atómica del Cu = 63,5.
 Entalpía
Entalpía