-
Reactivo limitante: cantidad de PCl3 que se obtiene (4885)
¿Qué masa de 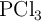 se forma en la reacción de 125 g de
se forma en la reacción de 125 g de 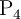 con 323 g de
con 323 g de 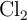 ?
?
La reacción que tiene lugar es:
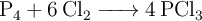
-
Reacción redox entre una aleación de cobre y ácido nítrico (6127)
Cuando se hacen reaccionar 200 g de una aleación, que contiene cobre en un 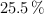 , con 180 mL de una disolución de ácido nítrico al
, con 180 mL de una disolución de ácido nítrico al 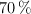 en masa y densidad 1.41 g/mL, se obtienen como productos de reacción óxido de nitrógeno(II), nitrato de cobre(II) y agua con un rendimiento del
en masa y densidad 1.41 g/mL, se obtienen como productos de reacción óxido de nitrógeno(II), nitrato de cobre(II) y agua con un rendimiento del 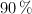 .
.
a) Ajusta la reacción que tiene lugar empleando el método del ion-electrón, indica cuál es el agente oxidante y el agente reductor, así como los estados de oxidación de las especies oxidadas y reducidas.
b) Calcula los gramos de nitrato de cobre(II) que se obtienen.
c) Si el óxido de nitrógeno(II) se recoge sobre agua a 293 K y 1 atm, calcula el volumen recogido.
Masas atómicas: Cu = 63.5 ; N = 14 ; O = 16 ; H = 1.
-
Masa de nitruro de litio a partir de masas iguales de reactivos (4773)
El litio y el nitrógeno reaccionan para producir nitruro de litio según a reacción:
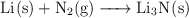
Si se hacen reaccionar 5 g de cada reactivo y el rendimiento es del 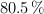 , ¿cuántos gramos de
, ¿cuántos gramos de 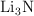 se obtendrán en la reacción?
se obtendrán en la reacción?
Masas atómicas: Li = 7 ; N = 14.
-
Reactivo limitante y masa de producto a partir de reactivos impuros (5499)
La siguiente es una reacción espontánea del aluminio metálico con bromo, un no metal líquido. La ecuación es la siguiente:
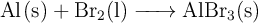
a) Si se hicieron reaccionar 12 g de aluminio (al 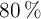 de pureza) y 56 g de bromo (al
de pureza) y 56 g de bromo (al 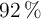 de pureza), ¿cuál es la sustancia que actúa como reactivo limitante?
de pureza), ¿cuál es la sustancia que actúa como reactivo limitante?
b) ¿Cuántos gramos de bromuro de aluminio se producen si el rendimiento de la reacción es del 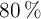 ?
?
Masas atómicas: Al = 27 y Br = 80.
-
Reacción formación del K2O: reactivo limintante y producto formado (5405)
Si usamos 50 g de potasio y 45 g de oxígeno para reaccionar y formar óxido de potasio:
a) ¿Cuánto producto se forma?
b) ¿Qué reactivo sobra y en qué cantidad?
c) ¿Qué masa del otro reactivo sería necesaria para que reaccionara la totalidad de los reactivos?
Masas atómicas: K = 39 ; O = 16
 Reactivo limitante
Reactivo limitante