-
Moles de producto y estequiometría en la combustión del amoniaco (2974)
De acuerdo con la reacción  , calcula cuántos moles de óxido de nitrógeno se obtienen a partir de 150 g de amoniaco.
, calcula cuántos moles de óxido de nitrógeno se obtienen a partir de 150 g de amoniaco.
Datos: N = 14 ; H = 1
-
Relación másica entre reactivo y producto 0001
¿Cuántos gramos de nitrito de sodio se obtienen a partir de 120 g de nitrato de sodio? La reacción que se da es:
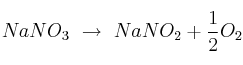
Datos: N = 14 ; O = 16 ; Na = 23
-
Relación entre moles de productos y reactivos 0001
¿Cuántos moles de nitrato de plata se necesitan para obtener 2,5 moles de cloruro de plata? La reacción a considerar es la siguiente:
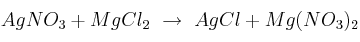
-
Ajustar y establecer estequiometría 0001
Determina la relación estequiométrica en la siguiente reacción química:
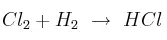
-
Estequiometría: reactivo limitante y rendimiento (2861)
Dada la siguiente reacción química, en la que se hacen reaccionar 36 g de 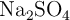 , con una pureza del
, con una pureza del 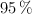 , y 27 g de
, y 27 g de 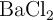 , con pureza del
, con pureza del 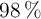 , y teniendo en cuenta que el rendimiento de la reacción es del
, y teniendo en cuenta que el rendimiento de la reacción es del 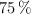 , calcula:
, calcula:

a) Ecuación balanceada.
b) El número de moles y gramos formados en la reacción.
Datos: Na = 23 ; Ba = 137.3 ; S = 32; O = 16 ; Cl = 35.5
 Reacciones químicas
Reacciones químicas