-
Reacciones químicas: relación volumétrica 0001
La siguiente reacción ocurre a temperatura y presión constantes. Observa la ecuación:
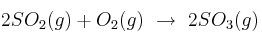
a) Determina cuántos litros de 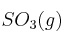 se forman cuando reaccionan 3 litros de oxígeno con suficiente cantidad de dióxido de azufre.
se forman cuando reaccionan 3 litros de oxígeno con suficiente cantidad de dióxido de azufre.
b) Si 3 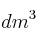 de dióxido de azufre reaccionan con 2
de dióxido de azufre reaccionan con 2 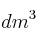 de oxígeno, ¿qué volumen de trióxido de azufre se forma?
de oxígeno, ¿qué volumen de trióxido de azufre se forma?
-
Reducción del óxido de cromo(III) (2857)
La reducción del 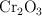 por el
por el 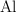 se realiza provocando la ignición de una mezcla adecuada y la reacción química es:
se realiza provocando la ignición de una mezcla adecuada y la reacción química es:

a) Ajusta la reacción.
b) ¿Cuántos gramos de cromo se obtienen con 250 g de 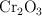 ?
?
Masas atómicas: Al = 27 ; Cr = 52 ; O = 16
-
Descomposición térmica de caliza: balanceo y pureza 0001
La caliza (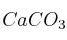 ) se descompone, calentándose, en cal viva (CaO) y dióxido de carbono.
) se descompone, calentándose, en cal viva (CaO) y dióxido de carbono.
a) Escribe la reacción química y ajústala.
b) Calcula el peso de cal viva que puede prepararse calentando 200 g de caliza con una pureza del 95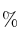 de
de 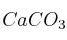 .
.
Masas atómicas: Ca = 40 ; C = 12 ; O = 16
-
Combustión del amoniaco: ajuste y reactivo limitante 0001
El amoniaco (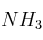 ) se quema para producir nitrógeno y agua:
) se quema para producir nitrógeno y agua:
a) Escribe y ajusta la reacción.
b) ¿Cuántos gramos de agua obtengo quemando 27 g de amoniaco?
c) Si quemo 20 g de amoniaco con 20 g de oxígeno, ¿cuántos gramos de nitrógeno obtengo?
-
Estequiometría y reactivo limitante en formación de urea (2854)
Según la reacción 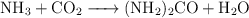 , hacemos reaccionar 500 g de amoniaco,
, hacemos reaccionar 500 g de amoniaco, 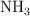 , con 750 g de
, con 750 g de 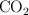 , para obtener urea.
, para obtener urea.
a) ¿Cuál de los dos es el reactivo limitante?
b) ¿Cuántos gramos de urea se obtienen supuesto un rendimiento del 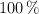 ?
?
 Reacciones químicas
Reacciones químicas