-
Relación estequiométrica con volúmenes y reactivo limitante 0001
En la reacción de formación de amoniaco (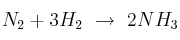 ), tenemos 50 litros de nitrógeno y 100 litros de hidrógeno,con P = 1 atm y T = 283 K. ¿Cuántos litros de amoniaco se obtienen?
), tenemos 50 litros de nitrógeno y 100 litros de hidrógeno,con P = 1 atm y T = 283 K. ¿Cuántos litros de amoniaco se obtienen?
-
Reacción química: reactivos gaseosos 0001
Se queman 20 L de sulfuro de hidrógeno en presencia de oxígeno para dar dióxido de azufre y agua. Escribe la reacción ajustada y determina el volumen de oxígeno necesario para quemar los 20 L de sulfuro de hidrógeno, suponiendo que la reacción se da en condiciones normales.
-
Estequiometría con reactivos gaseosos 0001
En la formación de esmog los gases nitrógeno y oxígeno reaccionan para formar dióxido de nitrógeno. ¿Cuántos gramos de 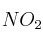 se producirán cuando reaccionen completamente 2,0 litros de nitrógeno a 840 mm Hg y a
se producirán cuando reaccionen completamente 2,0 litros de nitrógeno a 840 mm Hg y a 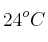 ?
?
-
Volumen de gas producido en una reacción química 0001
Al combinar 20 g de zinc con ácido clorhídrico para dar cloruro de zinc e hidrógeno. ¿Cuál es el volumen, en litros, de hidrógeno que se obtiene, medido en condiciones normales?
-
Aplicación de la nomenclatura inorgánica a las reacciones químicas (2360)
El sodio reacciona fácilmente con el oxígeno del aire formando un compuesto «X» quien, al adicionarle agua, origina otro compuesto denominado «Y». El compuesto «Y» reacciona totalmente con el ácido sulfúrico 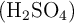 , produciendo una sal neutra «Z». Teniendo en cuenta la anterior información, escribe las reacciones químicas que tienen lugar y cuáles son las sustancias «X», «Y» y «Z».
, produciendo una sal neutra «Z». Teniendo en cuenta la anterior información, escribe las reacciones químicas que tienen lugar y cuáles son las sustancias «X», «Y» y «Z».
 Reacciones químicas
Reacciones químicas