-
PAU junio 2015 Andalucía: concentración y masa en el equilibrio y concentración
Para la reacción en equilibrio a 25 ºC: 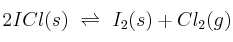 ,
, 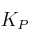 = 0,24. En un recipiente de 2 litros, en el que se ha hecho el vacío, se introducen 2 moles de
= 0,24. En un recipiente de 2 litros, en el que se ha hecho el vacío, se introducen 2 moles de 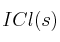 .
.
a) ¿Cuál será la concentración de 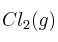 cuando se alcance el equilibrio?
cuando se alcance el equilibrio?
b) ¿Cuántos gramos de 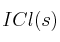 quedarán en el equilibrio?
quedarán en el equilibrio?
Datos: I = 127 ; Cl = 35,5 ; 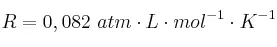
-
Constante de equilibrio y moles de especies 0001
En un recipiente de un 1 L, a temperatura ambiente, se introduce un mol de 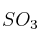 . Al analizarse el equilibrio según la ecuación:
. Al analizarse el equilibrio según la ecuación: 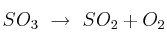 se comprueba que se han formado 0,6 mol de
se comprueba que se han formado 0,6 mol de 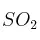 . Calcula el valor de la constante de equilibrio.
. Calcula el valor de la constante de equilibrio.
-
Constante de equilibrio para reacción heterogénea 0001
Establece la expresión de la constante de equilibrio para la reacción:
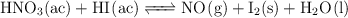
-
Constante de equilibrio inversa 0001
La constante de equilibrio para la reacción 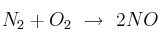 es
es 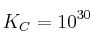 a 25 ºC. Calcula la constante de equilibrio inversa.
a 25 ºC. Calcula la constante de equilibrio inversa.
-
Selectividad junio 2014: solubilidad y producto de solubilidad
Se disuelve hidróxido de cobalto(II) en agua hasta obtener una disolución saturada a una temperatura dada. Se conoce que la concentración de iones 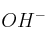 es
es 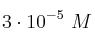 . Calcula:
. Calcula:
a) La concentración de iones 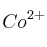 de esta disolución.
de esta disolución.
b) El valor de la constante del producto de solubilidad del compuesto poco soluble a esta temperatura.
 Constante equilibrio
Constante equilibrio