-
Ajuste de reacción y concepto de mol 0001
¿Qué masa de pentano (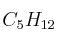 ) produce
) produce 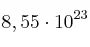 moléculas de
moléculas de 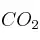 cuando se quema con oxígeno en exceso?
cuando se quema con oxígeno en exceso?
-
Estequiometría: masa de producto a partir de masas de reactivos 0001
Para obtener dióxido de estaño se han hecho reaccionar 8,32 g de estaño con 2,51 g de oxígeno. ¿Qué cantidad de óxido se formará?
Datos: Sn = 118,7 ; O = 16
-
Determinar la pureza de un reactivo (3051)
Una de las reacciones que se lleva a cabo en un alto horno donde el mineral de hierro se convierte en hierro fundido es:

Supón que se obtienen 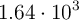 kg de Fe a partir de una muestra de
kg de Fe a partir de una muestra de 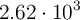 kg de
kg de 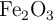 . Suponiendo que la reacción llegue a completarse, ¿cuál es la pureza, en tanto por ciento en masa, del
. Suponiendo que la reacción llegue a completarse, ¿cuál es la pureza, en tanto por ciento en masa, del 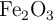 en la muestra original?
en la muestra original?
-
Reacción química: relación molar y másica entre sustancias 0001
En un alto horno, el trióxido de dihierro (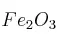 ) se hace reaccionar con carbón de coque (C) y se produce hierro fundido (Fe). Calcula el número de moles de hierro que se obtienen por cada kilogramo del óxido con que se alimente al horno. Escribe la ecuación química ajustada y obtén:
) se hace reaccionar con carbón de coque (C) y se produce hierro fundido (Fe). Calcula el número de moles de hierro que se obtienen por cada kilogramo del óxido con que se alimente al horno. Escribe la ecuación química ajustada y obtén:
a) La solución por el método de relación mol-mol.
b) La solución por el método de relación masa-masa.
-
Estequiometría: reactivo limitante y rendimiento (2861)
Dada la siguiente reacción química, en la que se hacen reaccionar 36 g de 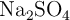 , con una pureza del
, con una pureza del 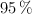 , y 27 g de
, y 27 g de 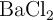 , con pureza del
, con pureza del 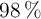 , y teniendo en cuenta que el rendimiento de la reacción es del
, y teniendo en cuenta que el rendimiento de la reacción es del 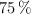 , calcula:
, calcula:

a) Ecuación balanceada.
b) El número de moles y gramos formados en la reacción.
Datos: Na = 23 ; Ba = 137.3 ; S = 32; O = 16 ; Cl = 35.5
 Mol
Mol