-
Estequiometría: Gases y disoluciones 0001
Se dispone de una disolución acuosa de HCl, cuya densidad es de 1,03 g/mL. Se toman 5 mL de esta disolución a los que se les va añadiendo cinc en polvo hasta que se observa que cesa el desprendimiento de gas, momento en el que se para la reacción y se mide que se han desprendido 70 mL de gas, medidos en c.n.
a) Indica la naturaleza del gas que se desprende.
b) Halla los gramos de cinc que han reaccionado en el HCl.
c) Halla la concentración en 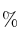 en peso de la disolución de HCl.
en peso de la disolución de HCl.
d) ¿Cuál es la molaridad y la molalidad de la disolución de HCl?
-
Problema disoluciones (1127)
Al disolver 4 g de una sustancia en 50 g de benceno se obtuvo una disolución que hierve a 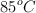 . Determina si la sustancia que se disolvió es metanal (
. Determina si la sustancia que se disolvió es metanal (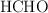 ) o etanal (
) o etanal (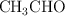 ).
).
Datos: 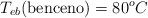 ;
; 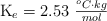 .
.
-
Masa molar de una sustancia conociendo el descenso crióscopico del benceno (1105)
Determina la masa molar de una sustancia si al disolver 17 g de la misma en 150 g de benceno se obtiene una mezcla que se congela a 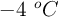 .
.
Datos: 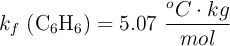 ;
; 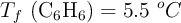
-
Problema disoluciones (1102)
Tenemos una disolución de ácido sulfúrico (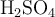 ) 2 M cuya densidad es 1.15 g/mL. Expresa su concentración como molalidad, fracción molar y porcentaje en masa.
) 2 M cuya densidad es 1.15 g/mL. Expresa su concentración como molalidad, fracción molar y porcentaje en masa.
Datos: H = 1 ; S = 32 ; O = 16.
-
Volumen de ácido comercial para preparar una disolución 0.4 N (245)
Se desea preparar 200 mL de ácido clorhídrico 0.4 N a partir de un ácido clorhídrico comercial de 1.18 g/mL de densidad y una riqueza del 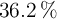 en peso. ¿Cuántos mL de ácido comercial se necesitan? Calcula la molaridad y la molalidad del ácido comercial.
en peso. ¿Cuántos mL de ácido comercial se necesitan? Calcula la molaridad y la molalidad del ácido comercial.
(Datos: H = 1 ; Cl = 35.5)
 Molalidad
Molalidad