-
PAU redox 0001
Sabiendo que la reacción del dicromato potásico con cloruro de estaño(II), en presencia de ácido clorhídrico, conduce a la obtención de cloruro de estaño(IV) y cloruro de cromo(III):
a) Ajusta la correspondiente ecuación molecular de oxidación-reducción.
b) Calcula la molaridad de la disolución de dicromato de potasio, sabiendo que 60 mL de la misma han necesitado 45 mL de una disolución de cloruro de estaño(II) 0,1 M para reaccionar completamente.
-
PAU electroquímica 0001
Para platear un objeto se ha estimado que es necesario depositar 40 g de plata.
a) Si se realiza la electrolisis de una disolución acuosa de sal de plata con una corriente de 2 amperios, ¿cuánto tiempo se tardará en realizar el proceso?
b) ¿Cuántos moles de electrones han sido necesarios para ello?
Datos: F =96500 C ; Ag =108.
-
PAU Ácido-base 0003
En medio acuoso, según la teoría de Brönsted-Lowry:
a) Justifica el carácter básico del amoniaco.
b) Explica si el 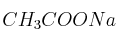 genera pH básico.
genera pH básico.
c) Razona si la especie 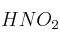 puede dar lugar a una disolución de pH > 7.
puede dar lugar a una disolución de pH > 7.
-
PAU: moles, moléculas y átomos de una masa de etano (882)
Un recipiente cilíndrico contiene 0.13 g de etano, calcula:
a) El número de moles de etano.
b) El número de moléculas de etano.
c) El número de átomos de carbono.
Datos: C =12 ; H = 1.
-
Ejercicio de formular y nombrar compuestos químicos (881)
Formula o nombra los siguientes compuestos: a) ácido crómico ; b) hidróxido de cobre(II) ; c) pentan-2-ol ; d) 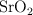 ; e)
; e) 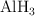 ; f)
; f) 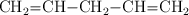
 EBAU
EBAU