-
Ordenar volúmenes de líquidos por el número de moles de cada uno (5572)
Se tienen los siguientes líquidos: 25.0 mL de 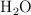 , 42.0 mL de
, 42.0 mL de 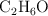 y 12.5 mL de
y 12.5 mL de 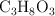 . Ordénalos, de forma decreciente a los moles de cada sustancia.
. Ordénalos, de forma decreciente a los moles de cada sustancia.
Densidades: 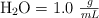 ,
, 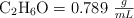 y
y 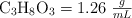 .
.
Masas atómicas: H = 1 ; C = 12 ; O = 16.
-
Molalidad de una disolución de glucosa (5529)
Al mezclar 30 g de glucosa (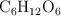 ) con 150 g de agua se obtienen 178 mL de disolución. Calcula la molalidad de la disolución.
) con 150 g de agua se obtienen 178 mL de disolución. Calcula la molalidad de la disolución.
Masas atómicas: C = 12 ; H = 1 ; O = 16.
-
Volumen de agua a partir de moles de la sustancia (5446)
Determina los litros de agua que se encuentran en 3.7 moles de la misma. Considera que la densidad del agua es 1 g/mL.
Masas atómicas: H = 1 ; O = 16.
-
Masa de siete moles del hidróxido doble de aluminio y sodio (5442)
Determina la masa en gramos de 7 moles de 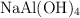 .
.
Masas atómicas: Na = 23 ; Al = 27 ; O = 16 ; H = 1.
-
Molaridad de una disolución de carnonato de sodio sabiendo masa y volumen
Determina la molaridad de una disolución que contiene 5 gramos de carbonato de sodio en 175 mL de disolución.
 Masa molecular
Masa molecular