-
EBAU Andalucía: química (junio 2022) - ejercicio C.3 (7936)
Se tiene una disolución de 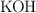 de
de 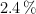 de riqueza en masa y
de riqueza en masa y 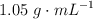 de densidad. Basándote en las reacciones químicas correspondientes, calcula:
de densidad. Basándote en las reacciones químicas correspondientes, calcula:
a) La molaridad y el pH de la disolución.
b) Los gramos de 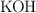 que se necesitan para neutralizar 20 mL de una disolución de
que se necesitan para neutralizar 20 mL de una disolución de 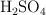 0.5 M.
0.5 M.
Masas atómicas relativas: K = 39 ; O = 16 ; H = 1.
-
Concentración de una disolución y agua necesaria para diluirla (7863)
Se dispone de 6.5 g de disolución acuosa de hidróxido de litio de 1.07 de densidad relativa y 0.08 de fracción molar en LiOH. Calcula:
a) La molalidad de la disolución.
b) La concentración en % en peso.
c) La molaridad de la misma.
d) ¿Cuántos gramos de agua habrá que añadir a la citada cantidad de disolución para que la fracción molar en LiOH sea ahora 0.04?
-
Masa y volumen de una disolución de bromano para preparar otra disolución (7839)
El bromano, a una concentración del 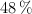 en masa, tiene una densidad de
en masa, tiene una densidad de 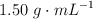 . ¿Qué masa y volumen de esta disolución serán necesarios para preparar 500 mL de una disolución 0.600 M? (Masas atómicas: Br = 80 ; H = 1).
. ¿Qué masa y volumen de esta disolución serán necesarios para preparar 500 mL de una disolución 0.600 M? (Masas atómicas: Br = 80 ; H = 1).
-
Volumen de HCl comercial necesario para hacer una disolución más concentrada (7792)
Estás trabajando en el laboratorio y necesitas preparar 1 L de HCl 1 M. Sin embargo, te has equivocado y has preparado 1 L de HCl 0.840 M. Como no debes desecharlo, indica qué volumen de HCl comercial debes añadir al litro preparado incorrectamente para conseguir una disolución 1 M teniendo en cuenta que tu HCl comercial tiene una concentración del 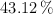 en masa y una densidad
en masa y una densidad 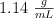 .
.
-
Concentración de catión calcio en una muestra de suero sanguíneo (7786)
Al analizar una muestra de suero sanguíneo se encuentra que contiene 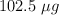 de
de 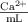 de suero. Si la densidad del suero es 1.053 g/mL y el peso atómico del calcio es 40.08, cuál es la concentración de
de suero. Si la densidad del suero es 1.053 g/mL y el peso atómico del calcio es 40.08, cuál es la concentración de 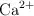 expresada en: a) molaridad b)
expresada en: a) molaridad b) 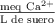 ; c) ppm de
; c) ppm de 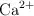 en peso?
en peso?
 Molaridad
Molaridad